
| A、①②③⑤ | B、②④⑤ |
| C、③④⑤ | D、②③⑥ |


科目:高中化学 来源: 题型:
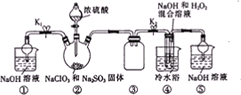 已知亚铝酸钠(NaClO2)为白色粉末,易溶于水,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2
已知亚铝酸钠(NaClO2)为白色粉末,易溶于水,NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
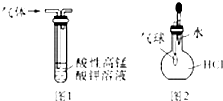
| A、用干燥pH试纸测定某新制氯水的pH |
| B、用25mL碱式滴定管量取20.00mL KMnO4溶液 |
| C、用图1装置除去乙烷中混有的乙烯 |
| D、用图2装置能验证HCl气体在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
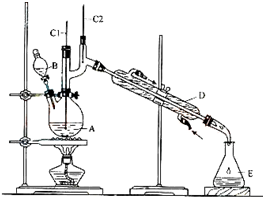 正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:
正丁醛是一种化工原料.某实验小组利用如下装置合成正丁醛.发生的反应如下:| Na2Cr2O7 |
| △H2SO4 |
| 沸点/℃ | 密度/g?cm-3 | 水中溶解性 | |
| 正丁醇 | 117.2 | 0.8109 | 微溶 |
| 正丁醛 | 75.7 | 0.8017 | 微溶 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、480mL容量瓶,称取7.68g硫酸铜,加入500mL水 |
| B、500mL容量瓶,称取12.0g胆矾配成500mL溶液 |
| C、480mL容量瓶,称取8.0g硫酸铜,加入500mL水 |
| D、500mL容量瓶,称取12.5g胆矾配成500mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
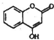 是一种医药中间体,常用来制备抗凝血药,可通过如图路线合成
是一种医药中间体,常用来制备抗凝血药,可通过如图路线合成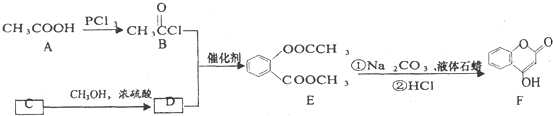
查看答案和解析>>
科目:高中化学 来源: 题型:
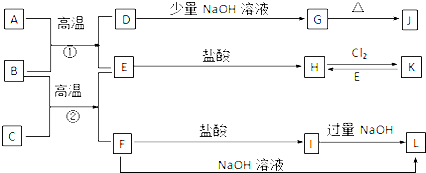
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在家用燃煤中加入适量的生石灰能有效减少二氧化硫的排放量 |
| B、研究采煤、采油新技术,尽量提高产量以满足工业生产的快速发展 |
| C、开发太阳能、水能、风能等新能源、减少使用煤、石油等化石燃料 |
| D、实现资源的“3R”利用,即:减少资源消耗(Reduce)、增加资源的重复使用(Reuse)、提高资源的循环利用(Recycle) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com