
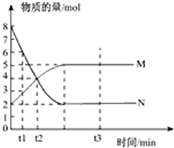
 一定温度下,在容积为1L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:
一定温度下,在容积为1L的密闭容器中进行反应:aN(g)?bM(g),M、N的物质的量随时间的变化曲线如图所示:分析 (1)根据物质的量的变化之比等于化学计量数之比求算;
(2)根据v=$\frac{△c}{△t}$计算M的平均反应速率;
(3)当反应达到平衡状态时,正、逆反应速率相等(同种物质),各物质的浓度、含量不再改变,以及由此衍生的一些物理量也不变,以此进行判断.
解答 解:(1)由图象可知,$\frac{a}{b}$=$\frac{△n(N)}{△n(M)}$=$\frac{(8-2)mol}{(5-2)mol}$=$\frac{6}{3}$=2,
故答案为:2;
(2)t1到t2时刻,以M的浓度变化表示的平均反应速率为:v=$\frac{△c(M)}{△t}$=$\frac{(5-4)mol}{\frac{1L}{({t}_{2}-{t}_{1})min}}$=$\frac{1}{({t}_{2}-{t}_{1})}$mol•L-1•min-1,
故答案为:$\frac{1}{({t}_{2}-{t}_{1})}$;
(3)A.平衡时反应混合物各组分的物质的量不变,但各组分的物质的量不一定相等,故A错误;
B.密闭容器中进行反应:aN(g)?bM(g),反应物、生成物都是气体,混合气体的总质量始终不变,混合气体总质量不变不能说明到达平衡,故B错误;
C.N的物质的量不再变化,说明可逆反应到达最大限度平衡状态,故C正确;
D.单位时间内消耗amolN,同时生成bmolM,都表示正反应速率,反应始终按此关系进行,不能说明到达平衡,故D错误;
故答案为:C.
点评 本题考查化学反应速率计算、化学平衡状态判断,题目难度不大,侧重对基础知识的巩固,注意判断化学平衡状态的物理量应随反应进行发生变化,该物理量由变化到不再变化说明到达平衡.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 +2Cu(OH)2+NaOH$\stackrel{△}{→}$
+2Cu(OH)2+NaOH$\stackrel{△}{→}$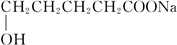 +Cu2O↓+3H2O.
+Cu2O↓+3H2O.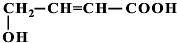 、
、 、
、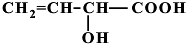 (提示:羟基不能连在碳碳双键上).
(提示:羟基不能连在碳碳双键上).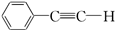 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 合成甲醇:CO+2H2$→_{加热加压}^{催化剂}$CH3OH | |
| B. | 合成乙醛:2CH2=CH2+O2$→_{加热加压}^{催化剂}$2CH3CHO | |
| C. | 合成有机玻璃单体-甲基丙烯酸甲酯: 第1步: 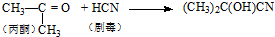 第2步: 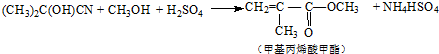 | |
| D. | 合成全降解聚碳酸酯塑料: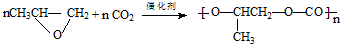 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
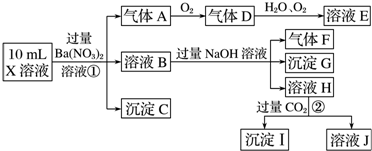
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
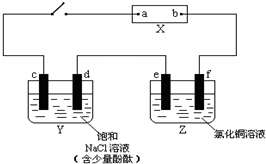
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)2溶于稀硝酸:Fe(OH)2+2H+═Fe2++2H2O | |
| B. | 等体积、等物质的量浓度的Ca(HCO3)2溶液和NaOH溶液混合:Ca2++2HCO${\;}_{3}^{-}$+2OH-═CaCO3↓+CO${\;}_{3}^{2-}$+2H2O | |
| C. | 硫酸亚铁溶液中加入用硫酸酸化的过氧化氢溶液:Fe2++2H++H2O2═Fe3++2H2O | |
| D. | 淀粉碘化钾溶液在空气变蓝:4I-+O2+2H2O═2I2+4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
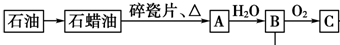
 ,它的一氯取代产物有2种.
,它的一氯取代产物有2种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com