
����Ŀ������������˵����Ӧ2A+B![]() 2C ( A��B��C��Ϊ���壩�ﵽƽ��״̬����
2C ( A��B��C��Ϊ���壩�ﵽƽ��״̬����
��A��B��C�İٷֺ�����ȣ�
�ڵ�λʱ���ڣ�����amolB��ͬʱ����2amo1C��
�۵�λʱ���ڣ�����amolA��ͬʱ����0.5amolB��
�������������ʱ���������������ٱ仯��
�������������ʱ�����������ʵ������ٱ仯��
��A��B��C�����ʵ���֮��Ϊ2 : 1 : 2
A. ������ B. ���ڢ��� C. �ڢܢ� D. �ۢ�
���𰸡�D
����������A��B��C�İٷֺ�����ȣ�����˵�����淴Ӧ������ȣ���һ������ƽ��״̬�����ڵ�λʱ���ڣ�����amolB��ͬʱ����2amo1C������ʾ����Ӧ���ʣ�����˵����Ӧ�ﵽƽ��״̬�����۵�λʱ���ڣ�����amolA��ͬʱ����0.5amolB��ʾ���淴Ӧ������ȣ��ﵽƽ��״̬����ȷ���ܸ��������غ㶨�ɿ�֪����������ʼ�ղ��䣬���ܾݴ�˵����Ӧ�ﵽƽ��״̬����������Ӧ�����С�������������ʱ�����������ʵ������ٱ仯��˵����Ӧ�ﵽƽ��״̬����ȷ����A��B��C�����ʵ���֮��Ϊ2 : 1 : 2������˵�����淴Ӧ������ȣ���һ������ƽ��״̬������ѡD��


 ��һ����ͬ���ɽ�����ϵ�д�
��һ����ͬ���ɽ�����ϵ�д� ������Ӧ���ϵ�д�
������Ӧ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�¶�ʱ,BaSO4��ˮ�еij����ܽ�ƽ����������ͼ��ʾ������˵����ȷ����( )
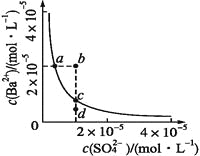
��ʾ:BaSO4(s)![]() Ba2+(aq)+SO42-(aq)��ƽ�ⳣ��Ksp=c(Ba2+)��c(SO42-),��Ϊ�ܶȻ�������
Ba2+(aq)+SO42-(aq)��ƽ�ⳣ��Ksp=c(Ba2+)��c(SO42-),��Ϊ�ܶȻ�������
A. ����Na2SO4����ʹ��Һ��a��䵽b��
B. ͨ����������ʹ��Һ��d��䵽c��
C. d����BaSO4��������
D. a���Ӧ��Ksp����c���Ӧ��Ksp
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���ȡ1mL PH=2�����ֶ�Ԫ��H2A��H2B���ֱ��ˮϡ�ͣ�PH�仯���ˮϡ�ͱ�������ͼ��ʾ�仯���������й�������ȷ����
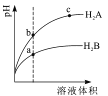
A. H2A�����Ա�H2B��
B. c����Һ�ĵ����Ա�a,b����Һ�ĵ����Զ�ǿ
C. ��0.1mol/LNaHA��Һ��PH=4������Ũ�ȴ�СΪc(Na+)>c(HA-)>c(A2-)>c(H2A) >c(H+)>c(OH-)
D. Na2B��ˮ��Һ�У�����Ũ�ȴ�СΪ�Ծ�c(Na+)>c(B2-)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��HCN(aq)��NaOH(aq)��Ӧ����H=��12.1kJ /mol��HCl(aq)��NaOH(aq)��Ӧ����H =��55.6kJ/ mol����HCN��ˮ��Һ�е���Ħ�H����
A����67.7 kJ /mol B����43.5kJ /mol C��+43.5 kJ/ mol D��+67.7 kJ/ mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���1L0.1mol��L-1NH4Cl��Һ��,���ϼ������NaOH��,NH4+��NH3��H2O�ı仯������ͼ��ʾ(��������Һ����ı仯�Ͱ��Ļӷ�)������˵����ȷ���ǣ� ��
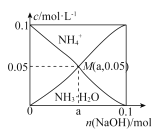
A. M����Һ��ˮ�ĵ���̶ȱ�ԭ��Һ��
B. a=0.05
C. ��n(NaOH)=0.05molʱ��Һ���У�c(Cl-)>c(Na+)>c(NH4+)>c(OH-)>c(H+)
D. ��M��ʱ,n(OH-)-n(H+)=(a-0.05)mol
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ȼ�ѧ����ʽ��д��ȷ��
A. �����ȼ����Ϊ-890 kJ/mol�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4(g)+2O2(g)=CO2(g)+ 2H2O(g)��H=-890 kJ/mol
B. ��һ�������½�1 molSO2��0.5molO2�����ܱ������г�ַ�Ӧ���ų�����79.2kJ,��Ӧ���Ȼ�ѧ����ʽΪ��2SO2(g)��O2(g)![]() 2SO3(g) ��H=��158.4kJ��mol��1
2SO3(g) ��H=��158.4kJ��mol��1
C. NaOH(s)��1/2H2SO4(Ũ)=1/2Na2SO4(aq)��H2O(l) ��H=��57.3kJ��mol��1
D. 2.00gC2H2������ȫȼ������Һ̬ˮ�Ͷ�����̼����ų�99.6kJ���������÷�Ӧ���Ȼ�ѧ����ʽΪ��2C2H2(g)��5O2(g)=4CO2(g)��2H2O(l) ��H=��2589.6kJ��mol��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ�뽺�������ص��ǣ� ��
A.����������������
B.��ֲ���͵���ˮ�����������γ���ˮ�����
C.���ö����ЧӦ����������Һ�뽺��
D.�ۿ���Ӱʱ���ӷ�ӳ������Ļ�����ԵĹ�·
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1�������������������ᣬ���᳧���ô���ԭ������β������������ʱ��H2��NO2��ԭΪN2��
��֪��2H2(g)+O2(g)��2H2O(g) ��H��-483.6kJ/mol
N2(g)+2O2(g)��2NO2(g) ��H��+67.7kJ/mol
��H2��NO2��ԭΪN2���Ȼ�ѧ��Ӧ����ʽ��__________________
��2��2SO2(g)+O2(g)![]() 2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1molSO2(g)����Ϊ1molSO3(g)����H= ��99kJ��mol����ش�����������
2SO3(g)��Ӧ���̵������仯��ͼ��ʾ����֪1molSO2(g)����Ϊ1molSO3(g)����H= ��99kJ��mol����ش�����������
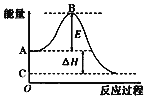
��ͼ��A���ʾ�� ��C���ʾ2mol SO3(g)����������E�������������� ��E�Ĵ�С�Ը÷�Ӧ�ķ�Ӧ�� (����������������)Ӱ�졣
��ͼ����H= ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش��������⣺�ϳɷ���Ȳ������ķ���֮һ���ڴ������£���Ȳ��ķ������屽������Ӧ���磺
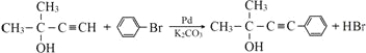
�� �� ��
������ʽ����ش�
��1���ķ���ʽ�� �����ܷ����ķ�Ӧ�� ��ѡ����ĸ����
a.ȡ����Ӧ b.�ӳɷ�Ӧ c.ˮ�ⷴӦ d.��ȥ��Ӧ
��2���Ա�Ϊԭ�������ҵĻ�ѧ����ʽ�� ��
��3���ɱ��Ʊ�![]() �ķ�Ӧ������ ��
�ķ�Ӧ������ ��
��4���������������ı���ͬ���칹���� �֣�������˳���칹����
�ٷ����г������ⲻ��������״�ṹ��
�ڱ�����ֻ��2��ȡ������������һ����ȩ����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com