
【题目】2018年11月《物理评论快报》报道了艾姆斯实验室制造的包含钙、钾、铁和砷以及少量镍的CaK(Fe1-xNix)4As4新型化合物材料,呈现出被称为刺猬自旋新磁态。有助于更好理解磁性 与非常规超导性之间的联系。回答下列问题:
(1)基态镍原子的价电子排布式为_______;上述材料中所含元素的基态原子中,未成对电子数最多的是_______ (填元素符号)。
(2)铁及其离子易形成配离子,如[Fe(CN)6]3-、[Fe(CN)x]4-、Fe(CO)5等。所包括的非金属元素中第一电离能最大的是______(填元素符号);[Fe(CN)6] 4-中含有σ键与π键的数目比为_____________。
(3)K3AsO3可用于碘的微量分析。
①AsO33-的立体构型为_______,写出一种与其互为等电子体的分子_______(填化学式)。
②K+的焰色反应呈紫色,金属元素能产生焰色实验的微观原因为_______。
(4)Ni与Ca处于同一周期,且核外最外层电子构型相同,但金属Ni的熔点和沸点均比金属Ca的高,其原因为_______。
(5)①金属镍的原子堆积方式如图所示,则金属镍晶胞俯视图为_______。

a.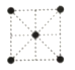 b.
b. c.
c. d.
d.
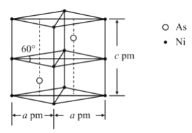
②某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为NA,该晶体的密度ρ=_____g·cm-3。
【答案】3d84s2 Fe N 1∶1 三角锥形 PCl3、PBr3、NF3、NCl3等 电子从较高能级的激发态跃迁到较低能级的激发态乃至基态时,会以光的形式释放能量 Ni的原子半径较小,价层电子数目较多,金属键较强 C ![]()
【解析】
(1)基态镍原子核外有28个电子,根据构造原理书写Ni原子的电子排布式,上述材料中所含元素为K、Ca、Ni、Fe、As,这些元素的基态原子中,未成对电子数分别是1、0、2、4、3;
(2)配离子含有Fe,C,N,O4种元素,非金属为C,N与O,原子轨道上电子处于全满、全空、半满时较稳定,结合C、N与O的电子排布式分析解答;
(3)①根据VSEPR理论判断AsO33-的立体构型,等电子体是指原子总数相同,价电子总数也相同的微粒;②电子从高能态跃迁到低能态时,要释放能量;
(4)金属晶体熔沸点的高低与金属键的强弱有关,金属键的强弱与价层电子数目和金属原子的半径有关;
(5)①根据图示,金属Ni的晶胞堆积方式呈现ABCABC……重复,这是面心立方最密堆积;②由晶胞结构结合均摊法,计算每个晶胞中含有的Ni原子和As原子个数,确定晶胞的质量,再根据晶体密度=晶胞质量÷晶胞体积计算。
(1)基态镍原子核外有28个电子, Ni原子的电子排布式为[Ar]3d84s2,
上述材料中所含元素为K、Ca、Ni、Fe、As,这些元素的基态原子中,未成对电子数分别是1、0、2、4、3,未成对电子数最多的是Fe,故答案为:3d84s2;Fe;
(2)配离子含有Fe,C,N,O4种元素,非金属为C、N与O,原子轨道上电子处于全满、全空、半满时较稳定,氮原子2p轨道上的电子为半充满,相对稳定,更不易失去电子,所以C、N、O这三种元素第一电离能最大的是N元素,[Fe(CN)6] 4-中含有6个配位键,6个C≡N,因此σ键与π键的数目比为(6+6)∶6×2=1∶1,故答案为:N;1∶1;
(3)①对于AsO33-,根据VSEPR理论,VP=BP+LP=3+![]() =4,则AsO33-的立体构型为三角锥形;等电子体是指原子总数相同,价电子总数也相同的微粒,与AsO33-互为等电子体的分子有:PCl3、PBr3、NF3、NCl3等,故答案为:三角锥形;PCl3、PBr3、NF3、NCl3等;
=4,则AsO33-的立体构型为三角锥形;等电子体是指原子总数相同,价电子总数也相同的微粒,与AsO33-互为等电子体的分子有:PCl3、PBr3、NF3、NCl3等,故答案为:三角锥形;PCl3、PBr3、NF3、NCl3等;
②电子从高能态跃迁到低能态时,要释放能量,所以金属焰色反应原理是激发态的电子从能量较高的轨道跃迁到能量较低的轨道时,以一定波长(可见光区域)光的形式释放能量,故答案为:电子从较高能级的激发态跃迁到较低能级的激发态乃至基态时,会以光的形式释放能量;
(4)Ni的原子半径较小,价层电子数目较多,金属键较强,故金属Ni的熔点和沸点均比金属Ca的高,故答案为:Ni的原子半径较小,价层电子数目较多,金属键较强;
(5)①根据金属镍的原子堆积模型图,金属Ni的晶胞堆积方式呈现ABCABC……重复,这是面心立方最密堆积,A选项是某一个面的二维图,俯视图中还可以看到C中相对于A多出的4个面心硬球,则金属镍晶胞俯视图为C,故答案为:C;
②由晶胞结构可知,Ni位于晶胞的顶点和4条棱上,每个晶胞中含有Ni原子数目=8×![]() +4×
+4×![]() =2,As位于晶胞内部,含有2个As原子,晶胞质量=2×
=2,As位于晶胞内部,含有2个As原子,晶胞质量=2×![]() g,晶胞的体积V=a×10-10 cm×a×10-10 cm×sin60°×c×10-10 cm=
g,晶胞的体积V=a×10-10 cm×a×10-10 cm×sin60°×c×10-10 cm=![]() ×10-30cm3,故晶胞的密度ρ=
×10-30cm3,故晶胞的密度ρ=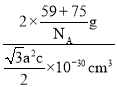 =
=![]() gcm-3,故答案为:
gcm-3,故答案为:![]() 。
。


 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】下列各组性质比较中,正确的是()
①沸点:![]()
②离子还原性:![]()
③酸性:![]()
④金属性:![]()
⑤气态氢化物稳定性:![]()
⑥半径:![]()
A.①②③B.③④⑤⑥C.②③④D.①③④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,能较长时间保持稳定的放电电压。高铁电池放电时总反应为3Zn+2K2FeO4+8H2O=3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是______。
(2)放电时,正极发生________(填“氧化”或“还原”)反应。
(3)负极电极反应式为______________,正极电极反应式为______________正极附近溶液的碱性_____(填“增强,减弱,不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁—次氯酸盐电池的工作原理如图,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-。下列有关说法正确的是( )
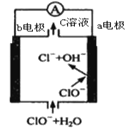
A.电池工作时,正极a附近的pH将不断增大
B.电池工作时,c溶液中的溶质是MgCl2
C.负极反应式:ClO-+2e-+H2O=Cl-+2OH-
D.a电极发生还原反应,每转移0.2mol电子,理论上生成0.2molCl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下列提供的一组物质回答问题:
①NH4Cl ②MgCl2 ③H2S ④Na2O2 ⑤MgO ⑥Cl2 ⑦NaOH ⑧H2O2 ⑨NH3 ⑩CO2
(1)既有极性共价键又有非极性共价键的是__(用序号表示)。
(2)既有离子键又有共价键的是__(用序号表示)。
(3)共价化合物有___(用序号表示)。
(4)CO2的电子式___;Na2O2的电子式__。
(5)用电子式表示MgCl2的形成过程:___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,将3molA和1molB两种气体混合于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)=xC(g)+2D(g)。2 min时测得生成0.8 mol D、0.4 mol C。下列判断不正确的是
A. x=1
B. 2 min时,A的浓度为0.9mol·L-1
C. 2 min内A的反应速率为0.3 mol·L-1·min-1
D. B的转化率为60%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某二元酸H2A在水溶液中发生电离:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。下列叙述不正确的是( )
H++A2-。下列叙述不正确的是( )
A. 在NaHA溶液中一定是:c(Na+)>c(HA-)>c(OH-)>c(H+)
B. 在Na2A溶液中一定是:c(Na+)>c(A2-)>c(OH-)>c(H+)
C. 在NaHA溶液中一定是:c(Na+)+c(H+)=c(HA-)+2c(A2-)+c(OH-)
D. 在H2A溶液中一定是:c(H+)=c(HA-)+2c(A2-)+c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝电池性能优越,Al-Ag2O2电池用于电解尿素[CO(NH2)2]的碱性溶液制备氢气(隔膜Ⅱ仅阻止气体通过,a、b均为惰性电极)。下列说法正确的是( )
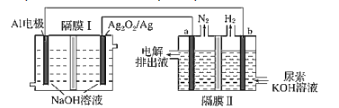
A.Ag电极是正极,反应后该电极区溶液pH减小
B.原电池的总反应为:2Al+3Ag2O2+2NaOH═2NaAlO2+3Ag2O+H2O
C.每消耗2.7g铝,理论上a、b两极共产生气体3.36L(标准状况)
D.a电极上的电极反应为:CO(NH2)2+8OH--6e-═CO32-+N2↑+6H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的分类或归类正确的一组是( )
①液氨、液氧、干冰、纯碱均为化合物 ②盐酸、氢氧化铁胶体、空气、氨水均为混合物 ③氢氧化钾、小苏打、硫酸、烧碱均为电解质 ④碘酒、牛奶、豆浆、肥皂水均为胶体 ⑤![]() 、
、![]() 、
、![]() 、
、![]() 均为钠盐
均为钠盐
A.①和②B.②和③C.②和④D.②③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com