
| A. | 常温常压下,11.2L氧气含氧分子数约为3.01×1023个 | |
| B. | 两个体积相同的容器,一个盛有NO,另一个盛有N2和O2的混合气体,在同温同压下两容器内气体分子总数、原子总数和气体质量也一定相等 | |
| C. | 标况下,等质量的O2和O3中所含的氧原子数目相等 | |
| D. | 将98gH2SO4溶于500ml水,得到溶液的物质的量浓度为2.0mol/L |
分析 A.常温常压下,气体摩尔体积大于22.4L/mol,则11.2L O2的物质的量小于0.5mol;
B.同温同压下,气体摩尔体积相等,体积相同的不同气体其物质的量相等,则分子数相等,结合摩尔质量;
C.氧气和臭氧是同素异形体,O原子的摩尔质量相等、质量相等,据此计算原子个数;
D.98g硫酸的物质的量是1mol,溶液的体积大于500mL,根据C=$\frac{n}{V}$计算物质的量浓度.
解答 解:A.常温常压下,气体摩尔体积大于22.4L/mol,则11.2L O2的物质的量小于0.5mol,则11.2L O2所含分子数小于3.01×1023个,故A错误;
B.同温同压下,气体摩尔体积相等,体积相同的不同气体其物质的量相等,则分子数相等,每个分子中原子个数相等所以原子总数相等,但两者的摩尔质量不等,所以气体质量不相等,故B错误;
C.氧气和臭氧是同素异形体,O原子的摩尔质量相等、质量相等,所以其原子个数相等,故C正确;
D.98g硫酸的物质的量是1mol,溶液的体积大于500mL,根据C=$\frac{n}{V}$知,其物质的量浓度小于2.0mol/L,故D错误;
故选C.
点评 本题考查阿伏伽德罗定律及其推论,侧重考查分析、计算能力,知道每个公式中各个物理量的含义即可解答,注意气体摩尔体积适用范围及适用条件,易错选项是C.


 天天练口算系列答案
天天练口算系列答案科目:高中化学 来源: 题型:选择题
| A. | 滴有碘水的淀粉溶液10ml分成两等份于两支试管,分别加入稀硫酸和唾液1ml,振荡,前者褪色快 | |
| B. | 恒温下,将盛有NO2和N2O4的平衡体系加压,体系颜色最终变浅 | |
| C. | 草酸溶液与酸性KMnO4溶液混合后,由于生成物对反应有催化作用,会使反应速率加快 | |
| D. | 在K2Cr2O7溶液中滴加浓硫酸,溶液颜色由橙色变黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3+HCl═NH4Cl | B. | 4NH3+5O2 $\frac{\underline{\;\;△\;\;}}{\;}$ 4NO+6H2O | ||
| C. | 3CuO+2NH3 $\frac{\underline{\;\;△\;\;}}{\;}$ 3Cu+N2+3H2O | D. | 8NH3+3Cl2 $\frac{\underline{\;\;△\;\;}}{\;}$ 6NH4Cl+N2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L H2O 的质量为18 g | |
| B. | 0.5 mol O2中含有的分子数约为6.02×1023 | |
| C. | 0.1 mol/L Na2CO3溶液中含Na+的物质的量为0.1 mol | |
| D. | 常温常压下,1.7 g NH3含有的质子数约为6.02×1023 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
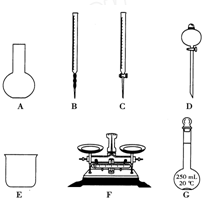 某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…
某化学兴趣小组测定某FeCl3样品(含少量FeCl2杂质)中铁元素的质量分数,实验按以下步骤进行:①称取ag样品,置于烧杯中;②加入适量盐酸和适量蒸馏水,使样品溶解,然后准确配制成250mL溶液;③准确量取25.00mL步骤②中配得的溶液,置于烧杯中,加入适量的氯水,使反应完全;④加入过量氨水,充分搅拌,使沉淀完全;⑤过滤,洗涤沉淀;⑥将沉淀转移到坩埚内,加热、搅拌,直到固体由红褐色全部变为红棕色后,在干燥器中冷却至室温后,称量;⑦…查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com