
下列反应中,硝酸既表现了氧化性又表现了酸性的是( )
A.C+浓HNO3 B.Cu+稀HNO3 C.CuO+浓HNO3 D.NaOH+HNO3
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源:2015-2016学年山东省高二下期中文科化学试卷(解析版) 题型:选择题
随着科学技术的不断进步,研究物质的手段和途径越来越多,H3、O4、C60 、N5+等已被发现。下列有关说法中,正确的是( )
A.H2与H3属于同素异形体 B.O2与O4属于同位素
C.C60的摩尔质量为720 D.N5+离子中含有36个电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年山东省高二下期中理科化学试卷(解析版) 题型:选择题
与CH2=CH2→CH2Br—CH2Br的变化属于同一反应类型的是( )
A.CH3CHO→C2H5OH
B.C2H5Cl→CH2=CH2
C.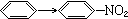
D.CH3COOH→CH3COOC2H5
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古包头市高一下期中化学试卷(解析版) 题型:选择题
A、B、C、D、E是同一周期的五种主族元素,A和B的最高价氧化物对应的水化物显碱性,且碱性B>A;C、D两种元素对应气态氢化物的稳定性C>D;E是这五种元素中形成简单离子半径最小的元素.则它们的原子序数由小到大的顺序为( )
A.D<C<E<A<B B.A<B<C<D<E C.E<B<A<C<D D.B<A<E<D<C
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古包头市高一下期中化学试卷(解析版) 题型:选择题
下列叙述中正确的是( )
A.最外层有2个电子的原子都是金属原子
B.除短周期外,其他周期均有18个元素
C.副族元素中没有非金属元素
D.碱金属元素是指IA族的所有元素
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古包头市高一下期中化学试卷(解析版) 题型:选择题
下列装置所示的实验中,能达到实验目的是( )
A.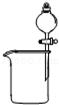 分离碘酒中的碘和酒精
分离碘酒中的碘和酒精
B.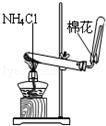 实验室制氨气
实验室制氨气
C. 除去Cl2中的HCl
除去Cl2中的HCl
D.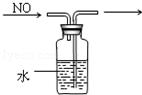 排水集气法收集NO
排水集气法收集NO
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高二下期中化学A卷(解析版) 题型:简答题
某含苯环的化合物A,其相对分子质量为104,碳的质量分数为92.3%。
(1)A的分子式为________________________;
(2)A与溴的四氯化碳溶液反应的化学方程式为______________________________。
(3)已知: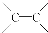
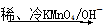
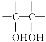 。 请写出A与稀、冷的KMnO4溶液在碱性条件下反应生成物的结构简式___________________________________;
。 请写出A与稀、冷的KMnO4溶液在碱性条件下反应生成物的结构简式___________________________________;
(4)在一定条件下,A与氢气反应,得到的化合物中碳的质量分数为85.7%。写出此化合物的结构简式______________________________________;
(5)在一定条件下,由A聚合得到的高分子化合物的结构简式为__________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省冀州市高二下期中化学A卷(解析版) 题型:选择题
如图有机物分子中带“※”碳原子是手性碳原子(连有四个不同基团的碳原子)。该有机物分别发生下列反应,生成的有机物分子中不会含有手性碳原子的是( )
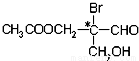
①与甲酸发生酯化反应
②与足量NaOH水溶液反应
③与银氨溶液作用只发生银镜反应
④催化剂作用下与H2反应
A.①②③④ B.①③
C.②④ D.以上反应都不成立
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二6月月考化学试卷(解析版) 题型:实验题
硫酸亚铁是重要的亚铁盐,在农业上用作农药,主要治小麦黑穗病,还可以用作除草剂;在工业上用于染色、制造蓝黑墨水和木材防腐等。
(1)新制的绿矾(FeSO4·7H2O)是浅绿色的,但在空气中极易变成黄色或铁锈色的碱式硫酸铁[Fe(OH)SO4],写出该反应的化学方程式: 。
(2)已知FeSO4在不同条件下分解得到产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2;SO3熔点是16.8℃,沸点是44.8℃。
某研究性学习小组拟用下列装置进行实验探究“在加热条件下FeSO4的分解产物”。
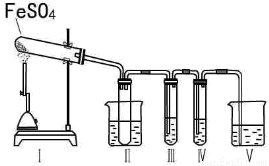
上述装置Ⅲ和Ⅳ用来检验气体产物。试回答下列问题:
①Ⅱ装置烧杯中水的温度应控制在 (选填“0℃、25℃、50℃”),装置Ⅱ的作用是 。
②装置Ⅲ中的试剂可以是 (选填序号,下同),现象是 ,则证明气体产物中含有SO3;装置Ⅳ中的试剂可以是 。
A.2mol/LNa2CO3溶液
B.品红溶液
C.0.5mol/L BaCl2溶液
D.0.5mol/LBa(NO3)2
E.0.01mol/L KMnO4溶液
F.淀粉碘化钾溶液
③装置V中试剂为NaOH溶液,发生反应的离子方程式为 。
④为了检验固体产物成分,取反应后的固体于试管中,加稀硫酸溶解,将所得溶液分成两份,进行如下实验:
操作步骤 | 预期实验现象 | 预期实验结论 |
向其中一份溶液中加入 | 固体中含有Fe2O3 | |
向另一份溶液中滴加2滴黄色K3[Fe(CN)6]溶液 | 产生蓝色沉淀 |
⑤若用22.8g FeSO4固体做实验,完全分解后,得到11.2g固体,其中Fe2O3的质量分数= (精确到0.1%)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com