

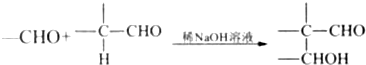
 .
. .肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是
.肉桂酸的同分异构体中,符合下列条件的有3种,其中在1H核磁共振谱图中出现信号峰数量最少的异构体的结构简式是 .
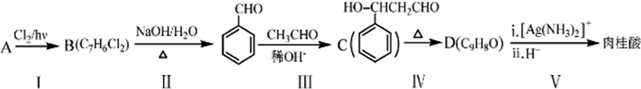
.分析 A与氯气在光照条件下与氯气发生取代反应生成B,B发生卤代烃的水解反应,再脱去1分子水得到 ,则A为
,则A为 ,B为
,B为 ,
, 与CH3CHO发生加成反应生成
与CH3CHO发生加成反应生成 ,C的分子式为C9H10O,对比C的结构与D的分子式可知,C脱去1分子水得到D,应是发生消去反应生成D,则D为
,C的分子式为C9H10O,对比C的结构与D的分子式可知,C脱去1分子水得到D,应是发生消去反应生成D,则D为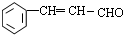 ,D与银氨溶液发生氧化反应、酸化得到肉桂酸,故肉桂酸的结构简式为
,D与银氨溶液发生氧化反应、酸化得到肉桂酸,故肉桂酸的结构简式为 ,据此解答.
,据此解答.
解答 解:A与氯气在光照条件下与氯气发生取代反应生成B,B发生卤代烃的水解反应,再脱去1分子水得到 ,则A为
,则A为 ,B为
,B为 ,
, 与CH3CHO发生加成反应生成
与CH3CHO发生加成反应生成 ,对比C的结构与D的分子式可知,C脱去1分子水得到D,应是发生消去反应生成D,则D为
,对比C的结构与D的分子式可知,C脱去1分子水得到D,应是发生消去反应生成D,则D为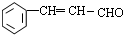 ,D与银氨溶液发生氧化反应、酸化得到肉桂酸,故肉桂酸的结构简式为
,D与银氨溶液发生氧化反应、酸化得到肉桂酸,故肉桂酸的结构简式为 .
.
(1)烃A为 ,名称为甲苯,故答案为:甲苯;
,名称为甲苯,故答案为:甲苯;
(2)则D为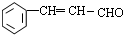 ,含有碳碳双键和醛基,故答案为:碳碳双键;醛基;
,含有碳碳双键和醛基,故答案为:碳碳双键;醛基;
(3) 与CH3CHO发生加成反应生成
与CH3CHO发生加成反应生成 ,C脱去1分子水得到D,应是发生消去反应生成D,故答案为:加成反应;消去反应;
,C脱去1分子水得到D,应是发生消去反应生成D,故答案为:加成反应;消去反应;
(4)步骤Ⅱ反应的化学方程式为 ,
,
故答案为: ;
;
(5)根据分析可知,肉桂酸的结构简式为: ,其同分异构体①既能发生银镜反应,又能发生水解反应,说明含有甲酸酯基;②碱性条件下水解时,1mol该异构体最多消耗2molNaOH,说明含有的酯基为酚羟基形成的酯基;③结构中除苯环外不含其它环状结构,则另有碳碳双键;综上,苯环上有-CH=CH2,和-OOCH两种官能团,临间对三种同分异构体,其中在1H核磁共振谱图中出现信号峰数量最少的是在对位,故答案为:
,其同分异构体①既能发生银镜反应,又能发生水解反应,说明含有甲酸酯基;②碱性条件下水解时,1mol该异构体最多消耗2molNaOH,说明含有的酯基为酚羟基形成的酯基;③结构中除苯环外不含其它环状结构,则另有碳碳双键;综上,苯环上有-CH=CH2,和-OOCH两种官能团,临间对三种同分异构体,其中在1H核磁共振谱图中出现信号峰数量最少的是在对位,故答案为: ;3;
;3; .
.
点评 本题考查有机物推断、有机物的结构与性质、有机反应类型、有机反应方程式和限制条件同分异构体的书写等知识,注意根据反应条件及有机物结构进行推断,需要学生熟练掌握官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 加热分解NH4Cl固体可以制得NH3 | |
| B. | Fe2O3是碱性氧化物,常用作红色油漆和涂料 | |
| C. | 硅单质常用来制作光导纤维和太阳能电池 | |
| D. | 浓硫酸具有脱水性,可以干燥Cl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同温同压下,相同体积的物质,它们的物质的量一定相等 | |
| B. | 任何条件下,等物质的量的二氧化硫和一氧化碳所含的分子数一定相等 | |
| C. | 1L一氧化碳气体一定比1L氧气的质量小 | |
| D. | 等体积、等物质的量浓度的强酸中所含的H+数一定相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 和
和  D、35Cl和37Cl
D、35Cl和37Cl
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.8g | B. | 22.4g | C. | 21g | D. | 19.6g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入Mg能放出H2的溶液中:K+、Al3+、Cl-、SO42- | |
| B. | 存在较多的Fe3+的溶液中:HCO3-、Cl-、SO42- | |
| C. | 水电离产生的c(OH-)=1×10-10 mol/L的溶液中:Al3+、SO42-、NO3-、Cl- | |
| D. | 使甲基橙变红色的溶液中:Na+、AlO2-、NO3-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
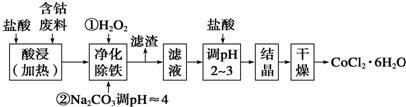
| 物质 | 溶度积Ksp | 沉淀完全时的pH |
| Co(OH)2 | 5.9×10-15 | 9.4 |
| Fe(OH)2 | 1.6×10-14 | 9.6 |
| Fe(OH)3 | 1.1×10-36 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
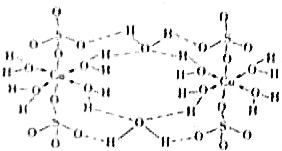 下列说法正确的是( )
下列说法正确的是( )| A. | 在如图结构示意图中,所有氧原子都采用sp3杂化 | |
| B. | 在如图结构示意图中,存在配位键、共价键和离子键 | |
| C. | 胆矾是分子晶体,分子间存在氢键 | |
| D. | 胆矾中的水在不同温度下会分步失去 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com