
在温度t℃下,某NaOH的稀溶液中c(H+)=10-a mol/L,c(OH-)=10-bmol/L,已知a+b=12,该温度下水的离子积Kw=________;t________25℃(填“大于”、“小于”或“等于”).向该溶液中逐滴加入pH=c的盐酸(t℃),测得混合溶液的部分pH如下表所示,假设溶液0混合前后的体积变化忽略不计,则c为________.

科目:高中化学 来源: 题型:
| 容器 编号 |
温度 /℃ |
起始量/mol | 平衡量/mol | 达到平衡的时间/min | 达平衡时体系能量的变化/kJ | ||
| CO | H2O | CO2 | H2 | ||||
| ① | 650 | 1 | 2 | 0.4 | 0.4 | 5 | 16.4kJ |
| ② | 650 | 2 | 4 | t1 | Q1 kJ | ||
| ③ | 900 | 2 | 4 | 1.6 | 1.6 | t2 | Q2 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 14 |
| 3 |
| 14 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
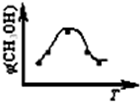 (2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料.
(2012?丹东模拟)能源短缺是人类面临的重大问题.甲醇是一种可再生能源.具有广泛的开发和应用前景.因此甲醇被称为21世纪的新型燃料.| 3 |
| 2 |
| 3 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 锥形瓶中溶液 | 滴定管 中溶液 |
选用 指示剂 |
选用 滴定管 | |
| A | 碱 | 酸 | 石蕊 | (乙) |
| B | 酸 | 碱 | 甲基橙 | (甲) |
| C | 碱 | 酸 | 酚酞 | (甲) |
| D | 酸 | 碱 | 酚酞 | (乙) |
查看答案和解析>>
科目:高中化学 来源: 题型:
I.下图为向25mL0.1mol/L NaOH溶液中逐滴滴加0.2moL/L CH3COOH溶液过程中溶液pH的变化曲线
 |
(1)B点溶液呈中性,有人据此认为,在B点时NaOH与CH3COOH恰好完全反应,这种看法是否正确? (选填“是”或“否”)。若不正确,则二者恰好完全反应的点是在AB区间内还是BD区间内? (若正确,此问不答)
(2)关于该滴定实验,从下列选项中选出最恰当的一项


(3)在AB区间内,c(OH-)>c(H+),则c(OH-)与c(CH3COO-)的大小关系是
A.c(OH-)一定大于c(CH3COO-)
B.c(OH-)一定小于c(CH3COO-)
C.c(OH-)一定等于c(CH3COO-)
D.c(OH-)可能大于、小于或等于C(CH3COO-)
(4)在D点时,溶液中c(CH3COO-)+c(CH3COOH) 2c(Na+)。(填“>”、“<”或“=”)
Ⅱ.在温度t℃时,某NaOH稀溶液中c(H+)=10-amol/L,c(OH-)=10-bmol/L,已知a+b=12,则:
(5)该温度下水的离子积常数Kw=
(6)该NaOH稀溶液中NaOH物质的量浓度的精确值是 mol/L(用含字母的表达式表示)
(7)在该温度下(t℃),将100mL 0.1mol/L的稀H2SO4溶液与100mL0.4mol/L的NaOH溶液混合后,溶液的pH=
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com