
| A. | 改变压强不一定改变反应速率 | |
| B. | 使用催化剂能同时增大正、逆反应的速率,并改变化学反应的限度 | |
| C. | 固体物质的状态(如块状、粉末状等)对反应速率有影响 | |
| D. | 升高温度一定能增大反应速率 |
分析 升高温度、加入催化剂可增大活化分子百分数,可增大反应速率,如增大压强,且浓度增大,则反应速率增大,增大固体表面积,也可增大反应速率,以此解答该题.
解答 解:A.恒温恒容下,通入不反应的气体,增大压强,反应气体物质的浓度不变,气体的反应速率不变,故A正确;
B.加入催化剂同等程度增大正逆反应速率,平衡不移动,故B错误;
C.增大固体表面积,增大接触面积,可增大反应速率,故C正确;
D.升高温度增大,增大活化分子百分数,增大单位体积内的活化分子数目,有效碰撞增大,反应速率加快,故D正确.
故选B.
点评 本题考查影响化学反应速率的因素,为高频考点,把握常见的影响反应速率的外界因素为解答的关键,注重基础知识的考查,选项A为解答的易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | Na2SiO3溶液与SO3的反应可用于推断Si与S的非金属性强弱 | |
| B. | NH4I的电子式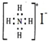 | |
| C. | 钠、锂分别在空气中燃烧,生成的氧化物中阴阳离子数目比不同 | |
| D. | Al2O3的化学键类型与AlCl3的化学键类型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.1mol/L | B. | 0.2mol/L | C. | 0.3mol/L | D. | 0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 如图所示为CH4燃料电池的装置(A、B为多孔碳棒):
如图所示为CH4燃料电池的装置(A、B为多孔碳棒):查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
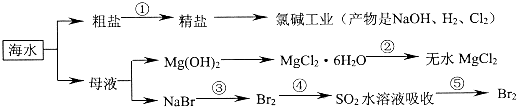
| A. | 以NaCl为工业原料可以生产烧碱、纯碱以及漂白粉等含氯产品 | |
| B. | 工业上通过电解饱和MgCl2溶液制取金属镁 | |
| C. | 第③④⑤步的目的是浓缩、富集溴单质,这三步中溴元素均被氧化 | |
| D. | 过程①除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的药品顺序为Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
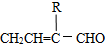 ,水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
,水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
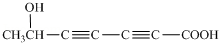 ;
;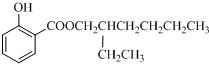 :
:查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com