
| A. | 标态下 22.4 升氧气 | |
| B. | 常温常压下 66 克的 CO2 | |
| C. | 1.2mol 的硫酸 | |
| D. | 100ml,0.1mol•L-1 的氢氧化钠溶液 |
分析 根据N=nNA可知,物质的量越大含有分子数越多,分别根据n=$\frac{V}{{V}_{m}}$=$\frac{m}{M}$计算出各物质的物质的量即可,注意氢氧化钠溶液中含有的分子为水分子.
解答 解:根据N=nNA可知,物质的量越大含有分子数越多,
A.标准状况下22.4L氧气的物质的量为:$\frac{22.4L}{22.4L/mol}$=1mol;
B.66g二氧化碳的物质的量为:$\frac{66g}{44g/mol}$=1.5mol;
C.1.2mol硫酸;
D.100mL0.1mol•L-1 的氢氧化钠溶液中含有的分子为水分子,且水分子的物质的量大于1.5mol;
根据分析可知,含有分子数目最多的为D,
故选D.
点评 本题考查了物质的量的计算,题目难度不大,明确物质的量与其它物理量之间的关系即可解答,D为易错点,注意氢氧化钠溶液中含有水分子,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:选择题
| A. | 分液时,先将上层液体从上口倒出 | |
| B. | 萃取时,振荡后,须打开活塞放气 | |
| C. | 蒸馏时,先点燃酒精灯,后通冷凝水 | |
| D. | 蒸发时,将溶剂蒸干一段时间后,熄灭酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属氧化物 氧化铁 FeO | B. | 酸性氧化物 二氧化硫 SO2 | ||
| C. | 酸 硫酸 H2SO4 | D. | 碱 纯碱 Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用惰性电极电解由X、Y、Z形成的化合物的水溶液,电解后溶液的pH值一定增大 | |
| B. | 由X、Y、Z形成的化合物的分子式一定为X2YZ3 | |
| C. | 由X、Y、Z形成的化合物的水溶液可能呈酸性、中性或碱性 | |
| D. | X元素形成的单质晶体可能为金属晶体,Y、Z两元素形成的单质晶体一定为分子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 冰融化,克服的是H2O的分子间作用力 | |
| B. | 同分异构现象存在,是有机化合物种类繁多的原因之一 | |
| C. | 在N2、CO2和SiO2物质中,都存在共价键,它们都是由分子构成 | |
| D. | Na2 O2属于离子化合物,该物质中存在离子键和共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
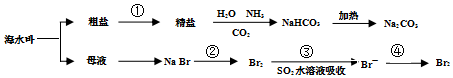
| A. | 工业上通过电解熔融状态MgCl2制取金属镁 | |
| B. | 用澄清石灰水可鉴别NaHCO3和Na2CO3 | |
| C. | 在第②、④步骤中,溴元素均被氧化 | |
| D. | 制取NaHCO3的反应中,利用了其溶解度在相同条件下小于NaCl的性质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
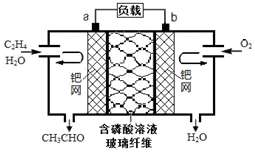 乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )
乙烯直接氧化法制乙醛的总反应方程式为2CH2═CH2+O2$\stackrel{PdCl_{2}•CuCl_{2}}{→}$2CH3CHO.下列有关说法正确的是( )| A. | 该电池可实现化学能与电能的相互转化 | |
| B. | 电子移动方向:电极a→磷酸溶液→电极b | |
| C. | 放电时,电路中每转移0.4mol电子,溶液中就有0.4molH+向负极迁移 | |
| D. | 该电池的负极反应式为:CH2═CH2-2e-+H2O=CH3CHO+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 短期保存Br2:盛于磨口的细口瓶中,并用水封,瓶盖严密 | |
| B. | 锂、钠、钾都保存在煤油中,密封 | |
| C. | 氨水、浓盐酸易挥发必须保存在棕色磨口细口瓶中 | |
| D. | 红磷无需密封保存 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com