
| A. | 用碘水可以鉴别葡萄糖溶液和淀粉溶液 | |
| B. | 淀粉、油脂和蛋白质在一定条件下都能发生水解反应 | |
| C. | 分子式为C2H6和C5H12的两种有机物一定互为同系物 | |
| D. | 向蛋白质溶液中加入浓的Na2SO4或CuSO4溶液均可使蛋白质盐析而分离提纯 |
分析 A、碘遇淀粉变蓝;
B、淀粉、油脂、蛋白质均可水解;
C、结构相似,组成上相差CH2原子团的有机化合物为同系物;
D、蛋白质溶液遇重金属盐发生蛋白质变性.
解答 解:A、碘遇淀粉变蓝,碘遇葡萄糖无变化,故A正确;
B、淀粉水解生成葡萄糖、油脂水解生成高级脂肪酸盐和甘油、蛋白质水解生成氨基酸,均可水解,故B正确;
C、分子式为C2H6和C5H12的两种有机物,符合通式CnH2n+2,为烷烃化合物,结构相似,组成上相差3个CH2原子团一定互为同系物,故C正确;
D、蛋白质溶液遇CuSO4溶液,发生蛋白质变性,故D错误;
故选D.
点评 本题考查了糖类、油脂、蛋白质的组成、结构和性质,合成纤维、胶体的性质等知识,涉及较为全面,掌握物质的性质是解题的关键.


科目:高中化学 来源: 题型:实验题
 为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.
为了研究外界条件对过氧化氢分解速率的影响,某同学做了以下实验,请回答下列问题.| 编号 | 操作 | 实验现象 |
| ① | 分别在试管A、B中加入5mL 5% H2O2溶液,各滴入2滴1mol/L FeCl3溶液.待试管中均有适量气泡出现时,将试管A放入盛有5℃左右冷水的烧杯中浸泡;将试管B放入盛有40℃左右热水的烧杯中浸泡. | 试管A中不再产生气泡; 试管B中产生的气泡量增大. |
| ② | 另取两支试管分别加入5mL 5% H2O2溶液和5mL 10% H2O2溶液 | 试管A、B中均未明显见到有气泡产生. |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

 +(2n-1)H2O.
+(2n-1)H2O.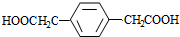 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{a}{2mol}$ | B. | $\frac{a}{22.4-b}$mol | C. | ($\frac{a}{22.4}$-$\frac{b}{2}$)mol | D. | $\frac{b}{2}$mol |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当消耗0.1 mol Zn时,得到的还原产物为0.1 mol | |
| B. | 反应结束时,可得到0.3 mol ZnSO4 | |
| C. | 当溶液中不再产生气泡时,溶液中大量存在的阳离子只有Zn2+ | |
| D. | 最后得到的金属单质为Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHCO3 | B. | Na2CO3 | C. | Ca(OH)2 | D. | NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 己烷的密度比水大,且难溶于水 | B. | 己烷在光照时能发生取代反应 | ||
| C. | 己烷在光照时能发生加成反应 | D. | 己烷不易燃烧,可作为灭火剂 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com