
| A、饮用酸性饮料 |
| B、在牙膏中添加适量的Ca2+离子 |
| C、少吃甜食 |
| D、在牙膏中加入氟化物添加剂 |


 名师点拨卷系列答案
名师点拨卷系列答案科目:高中化学 来源: 题型:
| ||
| A、24 g/mol |
| B、24 |
| C、64 g/mol |
| D、64 |
查看答案和解析>>
科目:高中化学 来源: 题型:
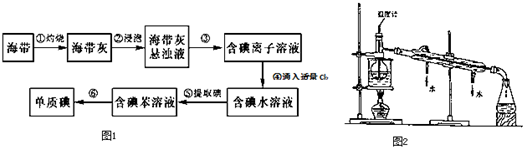
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | AgCl | Ag2SO4 | Ag2S | AgBr | AgI |
| 溶度积 | 1.8×10-10 | 1.4×10-5 | 6.3×10-50 | 5.0×10-13 | 8.3×10-17 |
| A、五种物质在常温下溶解度最大的是Ag2SO4 |
| B、向AgCl的悬浊液中加入0.1mol/L Na2S溶液,则可以生成黑色的Ag2S沉淀 |
| C、外界条件改变时,沉淀溶解平衡也会发生移动 |
| D、常温下,向AgI的悬浊液中加入0.1mol/L NaCl溶液,黄色沉淀变成白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用玻璃棒蘸取氯水溶液,滴在pH试纸上,待变色后与比色卡对照,确定氯水的pH |
| B、因为Ksp(CaCO3)<Ksp(CaSO4),所以可用Na2CO3和HCl除去水垢中的CaSO4 |
| C、均不能采取将溶液直接蒸干的方法制得AlCl3、Al2(SO4)3、FeCl3、Fe2(SO4)3 |
| D、滴定用的滴定管、锥形瓶和配制一定物质的量浓度溶液用的容量瓶,使用前均要润洗 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | Cu(OH)2 | Fe(OH)3 | CuCl | CuI |
| Ksp | 2.2×10-20 | 2.6×10-39 | 1.7×10-7 | 1.3×10-12 |

查看答案和解析>>
科目:高中化学 来源: 题型:
| 浓硫酸 |
| 170℃ |
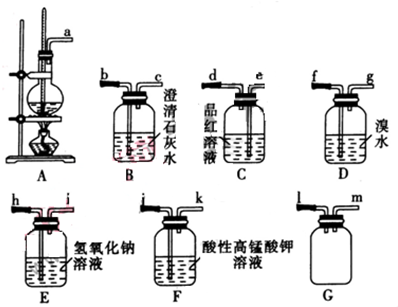
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不振荡,静置后上中下三层的颜色分别为无色、蓝色、紫色 |
| B、不振荡,静置后上中下三层的颜色分别为紫色、蓝色、紫色 |
| C、振荡,静置后溶液分为两层,水在下层 |
| D、振荡,静置后溶液仍分为三层 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com