
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A.24 g NaH中阴离子所含电子总数为NA |
| B.标准状况下,22.4 L苯中含有C—H键数目为6NA |
C.在碳酸钠溶液中,若c(C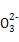 )="1" mol/L,则c(Na+)="2" mol/L )="1" mol/L,则c(Na+)="2" mol/L |
| D.通过MnO2催化使H2O2分解,产生32 g O2时转移电子数为2NA |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
下列用来表示物质变化的反应式中,错误的是
| A.钢铁腐蚀时可能发生的正极反应:2H2O + O2 + 4e- = 4OH- |
| B.向KHSO4溶液中滴入Ba(OH)2溶液使pH=7:SO42- + 2 H+ + Ba2+ + 2OH-= BaSO4↓+ 2 H2O |
C.明矾水解的离子方程式:Al3+ + 3H2O Al(OH)3 + 3H+ Al(OH)3 + 3H+ |
| D.K37ClO3与浓盐酸(HCl)在加热时生成氯气:K37ClO3 + 6HClΔ K37Cl + 3Cl2↑+ 3H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
NA为阿伏加德罗常数,下列叙述正确的是
| A.10 g H218O含有的中子数为5NA |
| B.1 mol羟基(-OH)含有的电子数为10NA |
| C.1 mol 氯气参加反应时,电子转移数目一定为2NA |
| D.标准状况下,11.2L己烷含有的分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列化学用语或模型表示不正确的是
A.中子数为14的硅原子: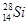 |
B.CH4分子的比例模型: |
C.聚乙烯的结构简式: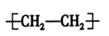 |
| D.次氯酸分子的结构式:H—O-Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
室温时,盐酸和硫酸的混合溶液20mL,向混合物中逐滴加入0.05mol/L Ba(OH)2溶液时,生成的BaSO4和pH的变化如图所示(不考虑溶液混合时体积的变化)。下列说法正确的是
| A.图中A点溶液的pH=1 |
| B.生成沉淀的最大质量为2.33g |
| C.原混合溶液中盐酸物质的量浓度为0.1mol/L |
D.当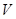 [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO [Ba(OH)2(aq)]=10mL时,发生反应的离子方程式为:Ba2++SO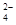 ═BaSO4↓ ═BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列溶液中,溶质的物质的量浓度不是1 mol/L的是( )
| A.10 g NaOH固体溶解在水中配成250 mL溶液 |
| B.将80 g SO3溶于水并配成1 L的溶液 |
| C.将0.5 mol/L的NaNO3溶液100 mL加热蒸发掉50 g水的溶液 |
| D.标准状况下,将22.4 L氯化氢气体溶于水配成1 L溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
标准状况下,m1g气体A与m2g气体B的分子数相等,下列说法中正确的是( )
A.1个A分子的质量是1个B分子的质量的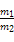 倍 倍 |
B.同温同体积的A与B的质量比为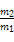 |
C.同温同质量的A与B的分子数比为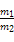 |
D.同温同压下A与B的密度比为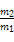 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关一定物质的量浓度的溶液配制的过程中,造成所得的溶液浓度偏大的是( )。
| A.要配制100 mL 1 mol·L-1 NaOH溶液,需在白纸上称4 g NaOH固体,并且称量速度较慢 |
| B.称量时托盘天平的砝码已被锈蚀 |
| C.溶解或稀释溶质时烧杯尚未干燥 |
| D.定容时盖上瓶盖,摇匀后发现液面低于刻度线,再继续滴加蒸馏水使液面重新达到刻度线 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
用NA表示阿伏加德罗常数的值。下列叙述正确的是( )
| A.2.24 L CH4气体中含有的电子数为NA |
| B.25 ℃时,1.0 L pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA |
| C.0.1NA个氯气分子溶于水形成1 L溶液,所得溶液中c(Cl-)="0.1" mol/L |
| D.1 mol CH3COONa和少量CH3COOH溶于水形成的中性溶液中,CH3COO-数目为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com