
| A. | 在原电池的负极和电解池的阴极上都发生失电子的氧化反应 | |
| B. | 原电池是自发的氧化还原反应,电解池发生的是不自发的氧化还原发应 | |
| C. | 电解精炼铜时,同一时间内阳极溶解铜的质量比阴极析出铜的质量大 | |
| D. | 镀层破损后,镀锡铁板比镀锌铁板更耐腐蚀 |
分析 A.原电池的负极失去电子发生氧化反应,正极得到电子发生还原反应;电解池中的阳极失去电子发生氧化反应,阴极得到电子发生还原反应;
B.电解反应不一定为非自发进行的氧化还原反应;
C.根据阳极材料组成以及电极反应分析判断;
D.镀层破损后,镀锡铁板中铁加快腐蚀,镀锌铁板中铁被保护.
解答 解:A.原电池中,负极失电子发生氧化反应,电解池中阴极得到电子发生还原反应,故A错误;
B.原电池的反应必须是自发的氧化还原反应,从理论上来讲,任何自发的氧化还原反应均可设计为原电池;而电解池反一般是非自发进行的氧化还原反应,故B正确;
C.电解精炼铜时,因为粗铜含有杂质,所以开始通电一段时间后,阳极溶解的铜的质量比阴极析出的铜的质量少,故C错误;
D.铁、锡和合适的电解质溶液构成的原电池中,铁作负极,易被腐蚀,锌、铁和合适的电解质溶液构成的原电池中,锌作负极,铁作正极被保护,所以镀锌铁板比镀锡铁板更耐腐蚀,故D错误;
故选B.
点评 本题考查原电池与电解池工作原理,题目难度不大,掌握基础知识是解题的关键,试题培养了学生的灵活应用能力.


科目:高中化学 来源: 题型:实验题
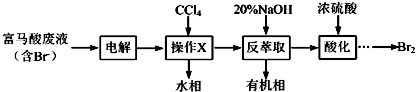
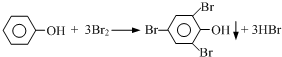
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 操作 | 结论 |
| A | 配制FeCl2溶液时加入适量的盐酸 | 抑制Fe2+水解 |
| B | 浓硫酸和蔗糖反应产生的气体通过足量的KMnO4溶液,气体全部被吸收且溶液紫红色褪去 | “黑面包实验”产生的气体具有还原性 |
| C | 制备乙酸乙酯的实验,将蒸出的乙酸乙酯蒸汽导在饱和的NaOH溶液液面以上 | 防止倒吸,便于分层. |
| D | 幼儿使用含NaF的牙膏,可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F,防止蛀牙 | Ksp[Ca5(PO4)3F]<Ksp[Ca5(PO4)3OH] |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| t/min | 2 | 4 | 7 | 9 |
| n(Y)/mol | 0.12 | 0.11 | 0.10 | 0.10 |
| A. | 反应前2min的平均速率v(Z)=2.0×10-3 mol/(L•min) | |
| B. | 其他条件不变,降低温度,平衡向正反应方向移动 | |
| C. | 当进行4分钟时,反应已达平衡状态 | |
| D. | 其他条件不变,通过缩小容器体积增大压强,平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | “低碳”意指更低的二氧化碳气体的排放 | |
| B. | 太阳能、水能、风能都属于可再生能源 | |
| C. | 太阳能电池的工作原理是光能与化学能的转换 | |
| D. | 利用燃气轮机进行天然气发电不属于可再生能源利用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| B12结构单元 | SF6 | S8 | HCN |
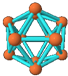 | 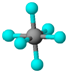 | 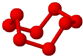 | 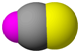 |
| 熔点1873K | 气体 | 易溶于CS2 | 溶液显弱酸性 |
| A. | 单质B12形成的晶体可能为原子晶体 | |
| B. | SF6是由极性键构成的非极性分子 | |
| C. | S8和HCN形成晶体后,晶体类型相同 | |
| D. | HCN形成晶体后,晶体中的作用力只有共价键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2O、Na2O2组成元素相同,含有的阴、阳离子数目之比也相同 | |
| B. | 金属钠着火时,可用泡沫灭火器来灭火 | |
| C. | 钠与熔融的四氯化钛反应可制取钛 | |
| D. | 实验时用剩的钠块应该放回原试剂瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com