
(16分)以黄铜矿为主要原料来生产铜、铁红颜料和硫单质,原料的综合利用率较高。其主要流程如下:

回答下面问题:
(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。这种方法的缺点是要消耗大量的热能以及 (完成合理的一种即可)。
(2)过滤③得到的滤渣成分是 (填化学式)。
(3)反应Ⅰ~Ⅴ中,共有 个反应不属于氧化还原反应。
(4)溶液A中含有的溶质是 (填化学式)。
(5)写出反应Ⅰ的化学方程式 。
(6)①反应Ⅲ是FeCO3在空气中煅烧,写出化学方程式 。
②反应Ⅳ中发生反应的离子方程式 。
(1)SO2会导致大气污染(2分);(2)S(2分)(3)2(2分);
(4)CuCl2、 NaCl (2分)(5)CuFeS2 + 3FeCl3 = CuCl↓+ 4FeCl2 + 2S↓(3分);
(6)①4FeCO3 + O2  4CO2 + 2Fe2O3 (3分) ② Cl- + CuCl = [CuCl2]- (2分)。
4CO2 + 2Fe2O3 (3分) ② Cl- + CuCl = [CuCl2]- (2分)。
【解析】
试题分析:(1)从黄铜矿冶炼粗铜的传统工艺是将精选后的富铜矿砂与空气在高温下煅烧,使其转变为铜。其中的S元素以SO2的形式出现,因此这种方法的缺点是要消耗大量的热能以及SO2导致大气污染;(2)向含有S、CuCl固体混合物中加入NaCl溶液,发生反应:CuCl+ NaCl=Na[CuCl2],不能发生反应,也不能在其中溶解的S单质仍然是以固体的形式存在,所以过滤③得到的滤渣成分是S;(3)在反应Ⅰ中FeCuS2中-2价的S与FeCl3中+3价的Fe发生氧化还原反应,S变为S单质,Fe则变为Fe2+,向FeCl2溶液中加入Na2CO3溶液发生复分解反应产生FeCO3和NaCl;所以反应II不是氧化还原反应;FeCO3在空气中煅烧,发生氧化还原反应产生Fe2O3,所以反应III是氧化还原反应,反应IV的方程式是CuCl+ NaCl=Na[CuCl2],在该反应中元素的化合价没有发生变化,不是氧化还原反应,因此这四个反应中共有2个反应不属于氧化还原反应。(4) Na[CuCl2]在溶液中发生歧化反应:2Na[CuCl2]=2NaCl+Cu+CuCl2,NaCl和CuCl2都溶于水,所以溶液A中含有的溶质是NaCl和CuCl2。(5)根据已知的反应物和生成物,结合原子守恒、电子守恒,可得反应Ⅰ的化学方程式是CuFeS2 + 3FeCl3 = CuCl↓+ 4FeCl2 + 2S↓;(6)①反应Ⅲ是FeCO3在空气中煅烧,发生氧化还原反应产生CO2和Fe2O3,根据电子守恒及原子守恒可得化学方程式是4FeCO3 + O2  4CO2 + 2Fe2O3;②反应Ⅳ中化学方程式是:CuCl+ NaCl=Na[CuCl2],将其改写为离子方程式是:Cl- + CuCl = [CuCl2]-。
4CO2 + 2Fe2O3;②反应Ⅳ中化学方程式是:CuCl+ NaCl=Na[CuCl2],将其改写为离子方程式是:Cl- + CuCl = [CuCl2]-。
考点:考查以黄铜矿为主要原料来生产铜、铁红颜料和硫单质的工艺流程的知识。主要包括方案的评价、物质成分的确定、化学反应类型的判断及化学反应方程式、离子方程式的书写。
考点分析: 考点1:物质的制备 考点2:铁及其化合物 考点3:铜及其化合物 试题属性

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014-2015学年北京市丰台区高三一模理综化学试卷(解析版) 题型:选择题
NO2、O2和熔融KNO3可制作燃料电池,其原理如图,该电池在使用过程中石墨I电极上生成氧化物Y,Y可循环使用。下列说法正确的是
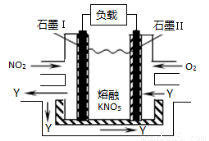
A.O2在石墨Ⅱ附近发生氧化反应
B.该电池放电时NO3-向石墨Ⅱ电极迁移
C.石墨Ⅰ附近发生的反应:3NO2 +2e- NO+ 2NO3-
NO+ 2NO3-
D.相同条件下,放电过程中消耗的NO2和O2的体积比为4∶1
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广西玉林市博白县高三下学期返校调研考试化学试卷(解析版) 题型:填空题
(14分)“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题。
(1)将不同量的CO(g)和H2O(g)分别通入到体积为2 L的恒容密闭容器中,进行反应CO(g)+H2O(g) CO2(g)+H2(g),得到如下三组数据:
CO2(g)+H2(g),得到如下三组数据:
实验组 | 温度℃ | 起始量/mol | 平衡量/mol | 达到平衡所需 | ||
CO | H2O | H2 | CO | |||
1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
3 | 900 | a | b | c | d | t |
①实验2条件下平衡常数K= 。
②实验3中,若平衡时,CO的转化率大于水蒸气,则a/b 的值_______(填具体值或取值范围)。
③实验4,若900 ℃时,在此容器中加入CO、H2O、CO2 、H2均为1 mol,则此时V正 V逆(填“<”,“>”,“=”)。
(2)已知在常温常压下:
①2CH3OH(l)+3O2(g) = 2CO2(g)+4H2O(g) ΔH=-1275.6 kJ·mol-1
②2CO (g)+ O2(g) = 2CO2(g) ΔH=-566.0 kJ·mol-1
③H2O(g) = H2O(l) ΔH=-44.0 kJ·mol-1
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:____________
(3)已知草酸是一种二元弱酸,草酸氢钠(NaHC2O4)溶液显酸性。常温下,向10 mL 0.01 mol·L-1 H2C2O4溶液中滴加10 mL 0.01 mol·L-1 NaOH溶液时,比较溶液中各种离子浓度的大小关系 ;
(4)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8×10-9。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为2×10-4 mol·L-1,则生成沉淀所需CaCl2溶液的最小浓度为 ______________mol·L-1。
(5)以二甲醚(CH3OCH3)、空气、H2SO4为原料,铂为电极可构成燃料电池,其工作原理与甲烷燃料电池的原理相似。请写出该电池负极上的电极反应式: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三高考测试(一)理综化学试卷(解析版) 题型:实验题
(16分)工业上用难溶于水的碳酸锶(SrCO3)粉末为原料(含少量钡和铁的化合物)制备高纯六水氯化锶晶体(SrCl2·6H2O),其过程为:

已知:Ⅰ.有关氢氧化物沉淀的pH:
氢氧化物 | Fe(OH)3 | Fe(OH)2 |
开始沉淀的pH | 1.5 | 6.5 |
沉淀完全的pH | 3.7 | 9.7 |
Ⅱ.SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
(1)操作①需要加快反应速率,措施有充分搅拌和 (写一种)。
碳酸锶与盐酸反应的离子方程式 。
(2)在步骤②-③的过程中,将溶液的pH值由1调节至 ;宜用的试剂为 。
A.1.5
B.3.7
C.9.7
D.氨水
E.氢氧化锶粉末
F.碳酸钠晶体
(3)操作③中所得滤渣的主要成分是 (填化学式)。
(4)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃ B.80~100℃ C.100℃以上
(5)步骤⑥宜选用的无机洗涤剂是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省湛江市高三高考测试(一)理综化学试卷(解析版) 题型:选择题
下列叙述正确的是
A.电解饱和食盐水能制得NaOH
B.澄清石灰水能鉴别Na2CO3和NaHCO3
C.配制溶液,定容时俯视容量瓶刻度会使溶液浓度偏低
D.铁粉中混入少量铝粉,可加入过量的氨水后过滤除去
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省、广雅中学、佛山一中高三联考理综化学试卷(解析版) 题型:实验题
(16分)硅孔雀石是一种含铜的矿石,含铜形态为CuCO3Cu(OH)2和CuSiO32H2O,同时含有SiO2、FeCO3、Fe2O3、Al2O3等杂质。以硅孔雀石为原料制取硫酸铜的工艺流程如下:
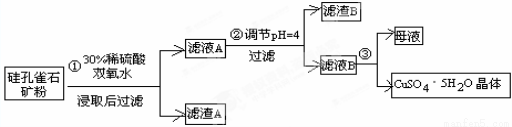
(1)步骤①中稀硫酸与CuSiO3·2H2O发生反应的化学方程式: ;
用离子方程式表示双氧水的作用_______________________________________。
(2)步骤②调节溶液pH选用试剂不可以是__________________
a.CuO b.Cu (OH)2 c.Cu2(OH)2CO3 d.CuSO4
(3)有关氢氧化物开始沉淀和完全沉淀的pH如下表:
氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 |
沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 |
由上表可知当溶液pH=4时,可以完全除去的离子是______(填金属离子符号,后同),不能完全除去的离子是________。
(4)滤液B通过蒸发浓缩(设体积浓缩为原来的一半)、冷却结晶、洗涤可以得到CuSO45H2O晶体。某同学认为上述操作会有硫酸铝晶体析出。请你结合相关数据,通过计算对该同学的观点予以评价 (填“正确”、“不正确”、或“无法判断”)
【已知常温下,Al2(SO4)3饱和溶液中c(Al3+)=2.25mol/L,Ksp[Al(OH)3]=3.2×10-34】
(5)测定硫酸铜晶体(CuSO45H2O)里结晶水的含量,实验步骤为:a.研磨;b.称量空坩埚和装有试样的坩埚的质量;c.灼烧;d.干燥器中冷却;e.称量;f.重复c至e的操作,直到连续两次称量的质量差不超过0.1g为止;⑦根据实验数据计算硫酸铜结晶水的含量。
①步骤c用到的仪器有酒精灯、三脚架、泥三角、玻璃棒、 、 。
②步骤f的目的是 。
③如灼烧后在空气中冷却再称量,结晶水的测定结果会____(填“偏高”、“低”或“不变”)
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省莆田市高三质量检测化学试卷(解析版) 题型:选择题
往含Cl-和I-的稀溶液中滴入AgNO3溶液,沉淀的质量与加入AgNO3溶液体积的关系如图所示。下列说法正确的是
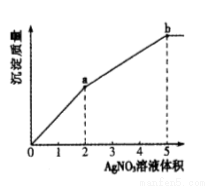
A.KSP (AgCl) < KSP (AgI)
B.c( Cl- ) :c( I-) = 3 :2
C.m( AgCl ) :m( AgI ) = 2 :3
D.a~b段产生黄色沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省盟校高三第一次十校联考理综化学试卷(解析版) 题型:实验题
(15分)硫代硫酸钠(Na2S2O3·5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。它易溶于水,难溶于乙醇,加热、遇酸均易分解。工业上常用亚硫酸钠法、硫化碱法等制备。某实验室模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如下图:
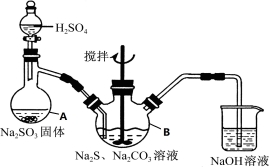
实验具体操作步骤为:
①开启分液漏斗,使硫酸慢慢滴下,适当调节分液的滴速,使反应产生的SO2气体较均匀地通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸。
②直至析出的浑浊不再消失,并控制溶液的pH接近7时,停止通入SO2气体。
③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3·5H2O。
④再经过滤、洗涤、干燥,得到所需的产品。
(1)写出仪器A的名称 步骤④中洗涤时,为了减少产物的损失用的试剂可以是 。
(2)为了保证硫代硫酸钠的产量,实验中不能让溶液pH<7,请用离子方程式解释原因 。
(3)写出三颈烧瓶B中制取Na2S2O3反应的总化学反应方程式 。
(4)最后得到的产品中可能含有Na2SO4杂质。请设计实验检测产品中是否存在Na2SO4,简要说明实验操作,现象和结论: 。
(5)测定产品纯度
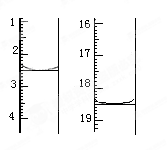
准确称取1.00 g产品,用适量蒸馏水溶解,以淀粉作指示剂,用0.100 0 mol·L-1碘的标准溶液滴定。反应原理为2S2O32-+I2===S4O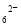 +2I-。滴定起始和终点的液面位置如图:则消耗碘的标准溶液体积为_______mL。产品的纯度为 %。
+2I-。滴定起始和终点的液面位置如图:则消耗碘的标准溶液体积为_______mL。产品的纯度为 %。
(6)Na2S2O3常用作脱氯剂,在溶液中易被Cl2氧化成SO42-,该反应的离子方程式为__________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com