
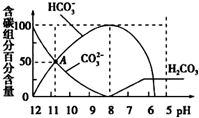
 常温下,在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L 盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.下列说法不正确的是( )
常温下,在20mL 0.1mol/L Na2CO3溶液中逐滴加入0.1mol/L 盐酸40mL,溶液的pH逐渐降低,此时溶液中含碳元素的微粒物质的量浓度的百分含量(纵轴)也发生变化(CO2因逸出未画出),如图所示.下列说法不正确的是( )| A、0.1 mol/L Na2CO3溶液中c(Na+)+c(H+)=2c(CO32-)+c(HCO3-)+c(OH-) |
| B、在A点:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| C、常温下CO2饱和溶液的pH约为5.6 |
| D、当加入20 mL盐酸时,混合溶液的pH约为8 |


科目:高中化学 来源: 题型:
| A、①③⑤ | B、②③ |
| C、②④ | D、①④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、②>④>③>① |
| B、②>④>①>③ |
| C、③>①>②>④ |
| D、①>④>③>② |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡常数约为0.3 |
| B、B的转化率为40% |
| C、A的平均反应速率为0.3 mol?(L?min)-1 |
| D、若混合气体的相对分子质量不变则表明该反应达到平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、A2+2B2=2AB2 |
| B、2A2+B2=2A2B |
| C、3A2+B2=2A3B |
| D、A2+3B2=2AB3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用米汤检验食用加碘盐中含有碘 |
| B、用醋、石灰水验证蛋壳中含有碳酸盐 |
| C、用碘酒检验葡萄中是否含有淀粉 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径的大小顺序:rY>rX>rQ>rW |
| B、X、Y的最高价氧化物的水化物之间不能发生反应 |
| C、Z元素的氢化物稳定性大于W元素的氢化物稳定性 |
| D、元素Q和Z能形成QZ2型的共价化合物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com