
 ,加聚反应.
,加聚反应. 分析 (1)乙烷与氯气发生取代反应生成一氯乙烷和HCl;
(2)乙烯与溴水发生加成反应生成1,2-二溴乙烷;
(3)乙烯不饱和的C=C双键中,其中1个C-C断裂结合水提供的-H、-OH,发生加成反应;
(4)乙烯中含碳碳双键,可发生加聚反应.
解答 解:(1)乙烷与氯气发生取代反应生成氯乙烷和HCl,该反应为:CH3CH3+Cl2$\stackrel{光照}{→}$C2H5Cl+HCl,
故答案为:CH3CH3+Cl2$\stackrel{光照}{→}$C2H5Cl+HCl;取代反应;
(2)乙烯含有碳碳双键,与溴水发生加成反应生成1,2-二溴乙烷,该反应为:CH2═CH2+Br2→CH2BrCH2Br,
故答案为:CH2═CH2+Br2→CH2BrCH2Br;加成反应;
(3)CH2=CH2中含有不饱和的C=C双键,能够在催化剂存在条件下与水发生加成反应生成乙醇,反应的化学方程式为:CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH,
故答案为:CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3CH2OH;加成反应;
(4)乙烯在一定条件下发生加聚反应生成聚乙烯,化学方程式为: ,
,
故答案为: ;加聚反应.
;加聚反应.
点评 本题考查化学反应方程式的书写,为高频考点,把握物质的性质及发生的化学反应为解答的关键,侧重烯烃及烷烃性质的考查,题目难度不大,注意取代与加成反应的不同.


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Z与X形成化合物的沸点高于Z的同族元素与X形成化合物的沸点 | |
| B. | 原子半径:Z>Y>X | |
| C. | CaY2与水发生氧化还原反应时,CaY2只作氧化剂 | |
| D. | CaY2和CaZ22种化合物中,阳离子与阴离子个数比均为1:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Al3+>O2- | B. | 与水反应的激烈程度:Al>Mg | ||
| C. | 热稳定性:HF>NH3 | D. | 单质的氧化性:S>O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 浓、稀硝酸都能使蓝色石蕊试纸最终变为红色 | |
| B. | 硝酸能与Cu反应,只表现氧化性 | |
| C. | 硝酸可与Na2S反应制得H2S气体 | |
| D. | 浓硝酸因分解放出的NO2又溶解于硝酸而呈黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烷和氯气按1:1混合,在光照下发生取代反应时,有机产物只有一种 | |
| B. | 在氧气中燃烧时只生成CO2和H2O的物质一定是烃 | |
| C. | 乙酸是有机弱酸,所以它的酸性比碳酸弱 | |
| D. | 在酯化反应中,羧酸脱去羧基中的羟基,醇脱去羟基中的氢而生成酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
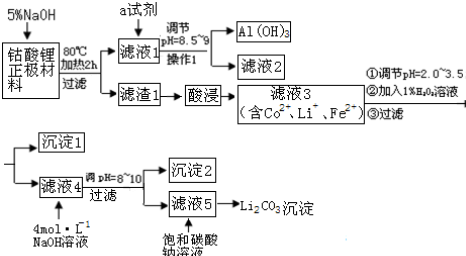
| 金属氢氧化物 | 金属离子浓度 1mol•L-1 | 金属离子浓度 0.1mol•L-1 | 沉淀完全时的pH值 | |
| 分子式 | Ksp | 开始沉淀时的pH | ||
| Fe(OH)2 | 4.87×10-17 | 5.8 | 6.3 | 8.3 |
| Fe(OH)3 | 2.79×10-39 | 1.2 | 1.5 | 2.8 |
| Co(OH)2 | 5.92×10-15 | 6.9 | 7.4 | 9.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com