
化学与生产生活密切相关,下列说法不正确的是
A.小苏打可用作糕点的膨化剂
B.二氧化硫可用作食品的漂白剂
C.PX(对二甲苯)是生成塑料、聚酯纤维和薄膜的主要原料
D.PM2.5指数是雾霾天气监测中的重要指标
1.B
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
玫瑰的香味物质中包含苧烯,苧烯的键线式为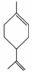 。
。
(1)1 mol苧烯最多可以跟________mol H2发生反应。
(2)写出苧烯跟等物质的量的Br2发生加成反应所得产物的可能的结构______________(用键线式表示)。
(3)有机物A是苧烯的同分异构体,分子中含有“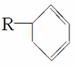 ”结构,A可能的结构为________________________________________________________________________
”结构,A可能的结构为________________________________________________________________________
___________________________________________________________(用键线式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是
A、 Na与H2O的反应是熵增的放热反应,该反应能自发进行
B、 饱和Na2SO4溶液或浓硝酸均可使蛋白质溶液产生沉淀,但原理不同
C、 FeCl3和MnO2均可加快H2O2分解,同等条件下二者对H2O2分解速率的改变相同
D、 Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s) Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
Mg2+(aq)+2OH—(aq),该固体可溶于NH4Cl溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl2·2H2O的流程如下:
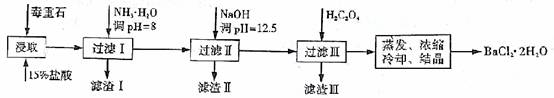
(1)毒重石用盐酸浸取前需充分研磨,目的是 。实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的 。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)
| Ca2+ | Mg2+ | Fe3+ | |
| 开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
| 完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
加入NH3·H2O调节pH=8可除去 (填离子符号),滤渣Ⅱ中含 (填化学式)。加入H2C2O4时应避免过量,原因是 。
已知:Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9
(3)利用简洁酸碱滴定法可测定Ba2+的含量,实验分两步进行。
已知:2CrO42—+2H+=Cr2O72—+H20 Ba2++CrO42—=BaCrO4↓
步骤Ⅰ 移取xml一定浓度的Na2CrO4溶液与锥形瓶中,加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mLBaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ 相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b mol·L-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。
滴加盐酸标准液时应用酸式滴定管,“0”刻度位于滴定管的 (填“上方”或“下方”)。BaCl2溶液的浓度为 mol·L-1,若步骤Ⅱ中滴加盐酸时有少量待测液溅出,Ba2+浓度测量值将 (填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
“ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为:NiCl2+2e-===Ni+2Cl-
D.钠离子通过钠离子导体在两电极间移动
查看答案和解析>>
科目:高中化学 来源: 题型:
用下列实验装置进行相应实验,装置正确且能达到实验目的的是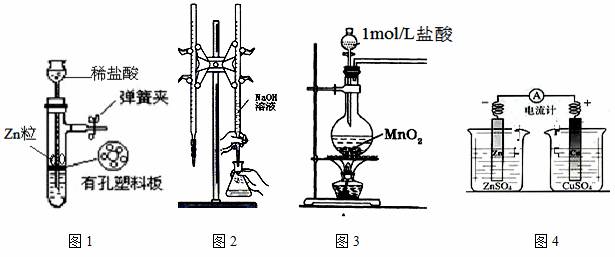
A.用图1所示装置制取少量H2
B.用图2所示装置用标准浓度的氢氧化钠溶液测定盐酸的浓度
C.用图3所示装置制取少量Cl2
D.用图4所示装置确定导线中有电流通过及并确定电流方向
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L恒容密闭容器中投入足量M(s)和一定量的R(g),发生反应为
M(s)+R(g) X(g)+Y(g)
X(g)+Y(g) 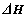 ;所得实验数据如下表所示:
;所得实验数据如下表所示:
| 实验 | 温度/℃ | 起始时R的物质的量/mol | 平衡时气体总物质的量/mol |
| ① | 300 | 2.00 | 2.80 |
| ② | 400 | 2.00 | 3.00 |
| ③ | 400 | 4.00 | a |
下列推断正确的是
A.上述反应中,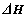 <0
<0
B.实验②中,该反应的平衡常数K=0.5
C.实验①经4 min达到平衡,0~4 min内υ(X)=0.2mol•L1•min1
D.实验③中a=6.00
查看答案和解析>>
科目:高中化学 来源: 题型:
[有机化学基础]
颠茄酸酯(J)是一种用于胃肠道平滑肌痉挛及溃疡病的辅助治疗药物,其合成路线如下:
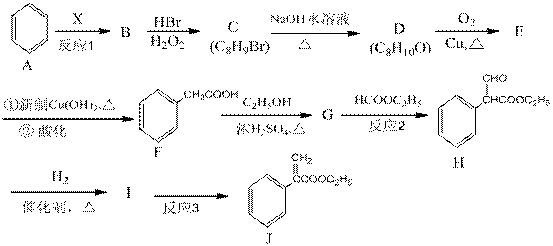
回答下列问题:
(1)烃B中含氢的质量分数为7.69%,其相对分子质量小于118,且反应1为加成反应,则B的分子式为___________,X的化学名称为 。
(2)C→D的反应类型为_____________,G→H 的反应类型为_____________。
(3)D的结构简式为___________________,G的结构简式为_______________________。
(4)反应3的化学方程式为_______________________________________________________。
(5)J的核磁共振氢谱有__________个峰。
(6)化合物I有多种同分异构体,同时满足下列条件的结构有 种。
①能发生水解反应和银镜反应
②能与FeCl3溶液发生显色反应
③苯环上有四个取代基,且苯环上一卤代物只有一种
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列化合物:
①NaCl、②NaOH、③HCl、④NH4Cl、⑤CH3COONa、⑥CH3COOH、⑦NH3·H2O、⑧H2O,回答下列问题。
(1)NH4Cl溶液显________性,用离子方程式表示原因________,其溶液中离子浓度大小顺序为________。
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=________,在pH=3的CH3COOH溶液中,水电离出来的c(H+)=________。
(3)已知纯水中存在如下平衡:H2O+H2OH3O++OH- ΔH>0,现欲使平衡向右移动,且所得溶液显酸性,可选择的方法是________(填字母序号)。
A.向水中加入NaHSO4固体
B.向水中加Na2CO3固体
C.加热至100 ℃[其中c(H+)=1×10-6 mol·L-1]
D.向水中加入(NH4)2SO4固体
(4)若将等pH、等体积的②NaOH溶液和⑦NH3·H2O溶液分别加水稀释m倍、n倍,稀释后两种溶液的pH仍相等 ,则m________(填“<”、“>”或“=”)n。
,则m________(填“<”、“>”或“=”)n。
(5)除⑧H2O外,若其余7种物质的溶液的物质的量浓度相同,则这7种物质的溶液按pH由大到小的顺序为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com