
【题目】下列说法中正确的是( )
A. 1molN2约含有6.02×1023个氮原子
B. 1mol H2O中含有2mol氢原子和1mol氧原子
C. 钠的摩尔质量就是它的相对原子质量
D. 硫酸的摩尔质量等于98g
 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源: 题型:
【题目】反应4A(g)+3B(g)═2C(g)+D(g),2min后B的浓度减少0.6molL﹣1.对2min内反应速率的表示正确的是( )
A. 用A表示的反应速率是0.3molL﹣1min﹣1
B. 分别用B、C、D表示的反应速率其比值为3:2:1
C. 在2min末的反应速率,用B表示是0.3molL﹣1min﹣1
D. 在2min内用B表示的反应速率的值是逐渐减小的,用C表示的反应速率的值是逐渐增大的
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知M2O7x- + 3 S2- + 14 H+ = 2 M 3+ + 3S ↓ + 7H2O,则M2O7x-中的M的化合价为( )
A. +2 B. +3 C. +4 D. +6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,将1mLpH=1的H2SO4溶液加水稀释到100ml,稀释后的溶液中![]() =______。
=______。
(2)某温度时,测得0.01mol/L的NaOH溶液的pH为11,则该温度下水的离子积常数KW=____,该温度______(填“高于”或“低于”)25℃。
(3)在(2)所述温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸Vb L混合。
①若所得混合液为中性,且a =12,b=2,则Va :Vb=____________。
②若所得混合溶液的pH=l0,且a=12,b=2,则Va :Vb=____________。
(4)常温下,设pH=5的H2SO4溶液中由水电离出的H+浓度为c1;pH=5是Al2(SO4)3溶液中由水电离出的H+浓度为c2,则![]() =________。
=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H=-QkJ/mol (Q>0) 在850℃时,K=1。
CO2(g)+H2(g) △H=-QkJ/mol (Q>0) 在850℃时,K=1。
①写出该反应的化学平衡常数的表达式K=__________。
②若升高温度到950℃,达到平衡时K____1 (填“大于”“ 小于”或“等于”),理由是__________。
③ 850℃时,若向一容积可变的密闭容器中同时充入1.0molCO,3.0molH2O,1.0molCO2和xmolH2,则:当x=5.0时,上述反应向_______________方向进行(填“正反应”或“逆反应”)。
④上述反应达平衡后,扩大该容器体积,平衡___________(正向移动、逆向移动或不移动)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化合物的叙述中正确的是
A.在共价化合物分子中一定同时存在σ键和π键
B.离子化合物的熔点一定比共价化合物的高
C.全由非金属元素组成的化合物一定是共价化合物
D.含有阳离子的化合物一定含有阴离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明矾石的主要成分是K2SO4Al2(SO4)32Al2O36H2O,还含有杂质Fe2O3 . 利用明矾石来制取纯净的Al2O3、K2FeO4和H2SO4的工艺流程如图所示. 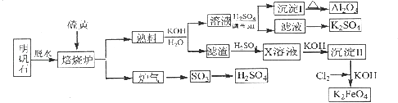
请回答下列问题:
(1)焙烧炉中发生反应的化学方程式为2Al2(SO4) ![]() 2Al2O3+6SO2↑+3O2↑,若生成102gAl2O3 , 转移的电子数目为 .
2Al2O3+6SO2↑+3O2↑,若生成102gAl2O3 , 转移的电子数目为 .
(2)生成沉淀I的离子方程式为 , 沉淀II的化学式为 .
(3)溶液经加硫酸调节pH后,过滤,洗涤,可得沉淀I,证明沉淀I已洗涤干净的实验操作和现象是
(4)写出Cl2将沉淀Ⅱ氧化为K2FeO4的化学方程式: .
(5)从滤液中得到K2SO4晶体的方法是 .
(6)K2FeO4也可以铁为电极,通过电解浓的KOH溶液来制取,写出电解法制取K2FeO4的阳极反应式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,可逆反应2NO2(g) ![]() 2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是 ①单位时间内生成nmolO2,同时生成2nmolNO2;②单位时间内生成nmolO2,同时生成2nmolNO;③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1;④混合气体的压强不再改变;⑤混合气体的颜色不再改变;⑥混合气体的平均相对分子质量不再改变。
2NO(g)+O2(g)在体积固定的密闭容器中反应,达到平衡状态的标志是 ①单位时间内生成nmolO2,同时生成2nmolNO2;②单位时间内生成nmolO2,同时生成2nmolNO;③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2∶2∶1;④混合气体的压强不再改变;⑤混合气体的颜色不再改变;⑥混合气体的平均相对分子质量不再改变。
A. ①④⑤⑥ B. ①③④⑥ C. ①②③⑤ D. ②⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com