
| A. | 人类目前所直接利用的能量大部分是由化学反应产生的 | |
| B. | 化学变化中的能量变化主要是由化学键变化引起的 | |
| C. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| D. | 能量变化是化学反应的基本特征之一 |
分析 A.当前能源结构中,燃料的燃烧是主要的能量来源;
B.根据化学变化中的能量变化主要是化学键的断裂与形成;
C.根据化学反应中能量变化的大小与反应物的质量有关;
D.根据化学反应的基本特征:产生新物质,能量发生变化分析.
解答 解:A.当前能源结构中,燃料的燃烧是主要的能量来源,燃烧反应为放热反应,所以人类目前所直接利用的能量大部分是由化学反应产生的,故A正确;
B.因化学变化中的能量变化主要是化学键的断裂与形成,故B正确;
C.因化学反应中能量变化的大小与反应物的质量有关,物质的质量越多,能量变化也越多,故C错误;
D.因化学反应的基本特征:产生新物质,能量发生变化,故D正确,
故选C.
点评 本题考查化学反应与能量变化,熟悉生活中的能源及与人类活动有关的能量变化是解答本题的关键,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 稀硫酸与0.1mol/LNaOH溶液反应:H+(aq)+OH-1(aq)═H2O(l)△H=-57.3kJ•mol-1 | |
| B. | 在101KPa下氢气的标准燃烧热△H=-285.5kJ•mol-1,则水分解的热化学方程式:2H2O(l)═2H2(g)+O2(g)△H=+285.5kJ•mol-1 | |
| C. | 已知2C(s)+O2(g)═2CO(g)△H=-221kJ•mol-1,则可知C的标准燃烧热为110.5kJ•mol-1 | |
| D. | 密闭容器中,9.6g硫粉与11.2g铁粉混合加热生成硫化亚铁17.6g时,放出19.12kJ热量,则Fe(s)+S(g)═FeS(s)△H=-95.6kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 定容时俯视观察液面 | |
| B. | 容量瓶中原有少量蒸馏水 | |
| C. | 溶解所用的烧杯、玻璃棒未洗涤 | |
| D. | 转移溶液时不慎将少量液体洒落在外 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
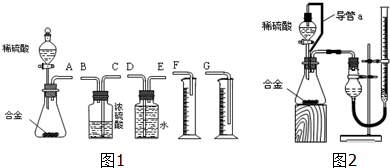
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图是某学校实验室从化学试剂商店买回的浓盐酸试剂标签上的部分内容.现用该浓盐酸配制250mL 2mol•L-1的稀盐 酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙; ⑤量筒;⑥托盘天平;⑦玻璃棒.请回答下列问题:
如图是某学校实验室从化学试剂商店买回的浓盐酸试剂标签上的部分内容.现用该浓盐酸配制250mL 2mol•L-1的稀盐 酸.可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙; ⑤量筒;⑥托盘天平;⑦玻璃棒.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质量相等,密度不等的N2和C2H4两种气体含有的分子数一定相等 | |
| B. | 同温同压下,等体积的H2和He气含有的质子数相等 | |
| C. | 某物质经分析仅含一种元素,此物质可能是纯净物也可能是混合物 | |
| D. | FeCl3溶液呈电中性,Fe(OH)3胶体带有电荷 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
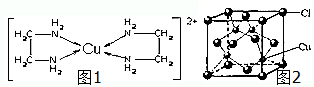 CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.已知:
CuCl和CuCl2都是重要的化工原料,常用作催化剂、颜料、防腐剂和消毒剂等.已知:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{(n-2m)}{V}mol•{L^{-1}}$ | B. | $\frac{(n-m)}{V}mol•{L^{-1}}$ | C. | $\frac{(2n-2m)}{V}mol•{L^{-1}}$ | D. | $\frac{(2n-4m)}{V}mol•{L^{-1}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2S+2HCl=H2S↑+2NaCl | B. | FeSO4+H2S=FeS↓+H2SO4 | ||
| C. | CuSO4+H2S=CuS↓+H2SO4 | D. | ZnS+2HCl=H2S↑+ZnCl2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com