
放射性同位素钬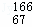 Ho的原子核内的中子数与核外的电子数之差是( )
Ho的原子核内的中子数与核外的电子数之差是( )
|
| A. | 32 | B. | 67 | C. | 99 | D. | 166 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列说法正确的是( )
A.将钠放入水中,钠将沉在水底
B.将一小块钠放在稀盐酸中,钠将与水反应生成NaOH和H2,生成的NaOH再与HCl反应生成NaCl和H2O
C.将一小块钠放在CuSO4溶液中发生如下反应:2Na+CuSO4═Na2SO4+Cu
D.Na2O和Na2O2中,氧元素化合价不同
查看答案和解析>>
科目:高中化学 来源: 题型:
要除去FeCl3溶液中混有少量的FeCl2,可加入 ,反应的离子方程式为 ﹣;要除去FeCl2溶液中的少量FeCl3,可加入铁粉,离子方程式为 +;要除去FeCl2溶液中的少量CuCl2,可加入 ,离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
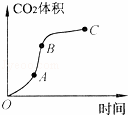
某学生用优质大理石与稀盐酸反应制取CO2,实验结果如下图所示,对于图中曲线的叙述正确的是( )
|
| A. | AB段表示反应速率最快 |
|
| B. | BC段表示反应速率最快,在该时间内收集到的气体最多 |
|
| C. | OC段表示随时间增加,反应速率逐渐增大 |
|
| D. | OC段表示反应产物中气体体积随时间的变化关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有一种微型电池,其电极分别为Zn和Ag2O,电解质溶液是KOH溶液,试回答下列问题:
(1)原电池是把 能转化成 能的装置.
(2)该电池中Zn极为 极.电极反应式为 .
(3)当金属Zn消耗了16.25g时,转移电子的物质的量为 mol.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子一定能大量共存的是( )
A.在无色溶液中:NH4+、Fe2+、SO42-、CO32- B.在含大量Ba2+的溶液中:NH4+、Na+、Cl-、OH-
C.在强碱溶液中:Na+、K+、Cl-、SO32- D.在pH =1的溶液中:K+、Fe2+、Cl-、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列反应的化学方程式,判断有关物质的还原性强
弱顺序是( )
①I2 + SO2 + 2H2O = H2SO4 + 2HI; ② 2FeCl2 + Cl2 = 2FeCl3;
③2 FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
FeCl3 + 2HI = 2FeCl2 + 2HCl+I2
A.SO2>I->Fe2+>Cl- B.Cl->Fe2+>SO2>I-
C.Fe2+>I->Cl->SO2 D.I->Fe2+>Cl->SO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com