
| A、焓变 | B、温度 | C、压强 | D、熵变 |
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、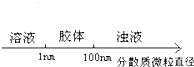 分散系的分类 |
B、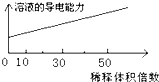 醋酸稀释 |
C、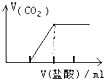 向Na2CO3溶液中逐滴滴入盐酸 |
D、 向AlCl3溶液中滴加过量的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(B2)=0.8mol?L-1?S-1 |
| B、v(B2)=0.42mol?L-1?S-1 |
| C、v(C)=0.6mol?L-1?S-1 |
| D、v(A2)=0.4mol?L-1?S-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NO2、SO2、NO和SO3四种气体的物质的量浓度之比为1:1:1:1 |
| B、生成n molSO2同时有n mol SO3消耗 |
| C、K值不再发生变化 |
| D、密闭容器中气体的密度不再发生变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2NO2(g)?N2O4(g)△H<0 |
| B、3O2(g)?2O3(g)△H>0 |
| C、H2(g)+I2(g)?2HI(g)△H<0 |
| D、NH4HCO3(s)?NH3(g)+H2O(g)+CO2(g)△H>0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
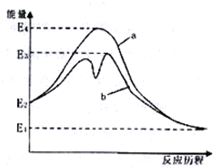 如图表示催化剂对某反应活化能的影响.几种酸的电离常数如下:HClO Kw=2.95×10-8,
如图表示催化剂对某反应活化能的影响.几种酸的电离常数如下:HClO Kw=2.95×10-8,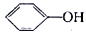 Kw=1.02×10-10H2CO3 Ka1=4.30×10-7 Ka2=5.61×10-11根据图象和数据判断,下列说法错误的是( )
Kw=1.02×10-10H2CO3 Ka1=4.30×10-7 Ka2=5.61×10-11根据图象和数据判断,下列说法错误的是( )| A、图说明了催化剂参与化学反应,并降低了活化能 |
| B、图中该反应没有催化剂参与时活化能为E2-E1 |
| C、将少量CO2通入NaClO溶液中,发生如下反应NaClO+CO2+H2O═HClO+NaHCO 3 |
D、相同浓度的NaClO溶液和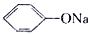 溶液,前者pH小 溶液,前者pH小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铝片与稀盐酸的反应 |
| B、Ba(OH)2.8H2O与NH4Cl的反应 |
| C、灼热的炭与CO2的反应 |
| D、甲烷在氧气中的燃烧反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| A、该反应是氧化还原反应 |
| B、MnO2发生还原反应 |
| C、HCl是还原剂 |
| D、若生成7.1 g Cl2,则转移0.1 mol电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com