
(1)工业合成氨时,合成塔中每产生1molNH3,放出46.1kJ的热量。
某小组研究在500℃下该反应过程中的能量变化。他们分别在体积均为VL的两个恒温恒容密闭容器中加入一定量的反应物,使其在相同温度下发生反应。相关数据如下:
容器 | 起始时各物质物质的量/mol | 达到平衡的时间 | 达平衡时体系能量的变化/kJ | ||
N2 | H2 | NH3 | |||
a | 1 | 4 | 0 | t1 min | 放出热量:36.88kJ |
b | 2 | 8 | 0 | t2 min | 放出热量:Q |
①容器a中,0~t1时间的平均反应速率为υ(H2)= ___________。
②下列叙述正确的是________(填字母序号)。
A.容器b中反应达平衡状态时,Q>73.76kJ
B.平衡时,两容器中H2的体积分数相等
C.反应开始时,两容器中反应的化学反应速率相等
D.平衡时,容器中N2的转化率:a<b
(2)以氨为原料,合成尿素的反应原理为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。
CO(NH2)2(l)+H2O(g) ΔH = a kJ·mol-1。
为研究平衡时CO2的转化率与反应物投料比[ ]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
]及温度的关系,研究小组在10 L恒容密闭容器中进行模拟反应。(Ⅰ、Ⅱ曲线分别表示在不同投料比时,CO2的转化率与温度之间的关系)。
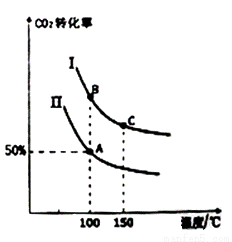
①a_______0 (填“>”或“<”)。
②若n(CO2)起始 =10 mol,曲线Ⅱ的投料比为0.4,在100℃条件下发生反应,达平衡至A点,则A点与起始压强比为_______。
③A点平衡常数与B点平衡常数间的关系:KA_______ KB (填“>”或“<”或“=”)。
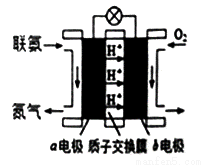
(3)利用氨气与空气催化氧化法制取联氨N2H4.如图是由“联氨—空气”形成的绿色燃料电池,以石墨为电极的电池工作原理示意图,b电极为_______极(填“正”或“负”),写出该电池工作时a电极的电极反应式_______。
 智能训练练测考系列答案
智能训练练测考系列答案 计算高手系列答案
计算高手系列答案科目:高中化学 来源:2016-2017学年新疆哈密地区第二中学高二上学期期末考试化学试卷(解析版) 题型:选择题
对于反应2NO2(g) N2O4(g) ΔH<0,达到平衡后缩小容器体积,下列说法正确的是
N2O4(g) ΔH<0,达到平衡后缩小容器体积,下列说法正确的是
A. 平衡逆向移动 B. 混合气体颜色比原来深
C. 混合气体颜色比原来浅 D. 混合气体的平均相对分子质量变小
查看答案和解析>>
科目:高中化学 来源:辽宁省大连市2017届高三3月双基测试化学试卷 题型:选择题
下列化学用语正确的有
①乙酸的最简式:CH2O
②二氧化硅的分子式:SiO2
③HClO的结构式:H—Cl—O
④乙烯是结构简式:CH2CH2
⑤Cl-的结构示意图: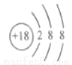
⑥过氧化钠的电子式:
⑦H2CO3的电离方程式:H2CO3 H++HCO3-
H++HCO3-
⑧吸氧腐蚀的正极反应:O2+4e-+4H+=2H2O
A. 1个 B. 2个 C. 3个 D. 4个
查看答案和解析>>
科目:高中化学 来源:2017届贵州省贵阳市高三2月适应性考试(一)理综化学试卷(解析版) 题型:实验题
纳米ZnO的颗粒直径介于1~100nm之间,具有许多特殊的性能,可用于制造变阻器、图像记录材料、磁性材料和塑料薄膜等。一种利用粗ZnO(含FeO、Fe2O3、CuO)制备纳米ZnO的生产工艺流程如下图所示:
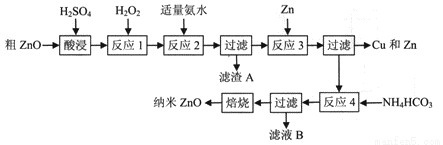
已知:① 生成氢氧化物沉淀时溶液的pH如下表:
物质 | Fe(OH)2 | Fe(OH)3 | Zn(OH)2 | Cu(OH)2 |
开始沉淀时pH | 6.34 | 1.48 | 6.2 | 5.2 |
完全沉淀时pH | 9.7 | 3.2 | 8.0 | 6.4 |
② 25℃时,Fe(OH)3的溶度积常数Ksp=4.0×10-38。
请回答以以下问题:
(1)酸浸时,为了提高浸出率,可采取的措施有________(填写两种);
(2)反应1中发生反应的离子方程式为______________,一种双氧水的质量分数为34.0 % (密度为1.13g/cm3) ,其浓度为_______mol/L;
(3)反应2中加适量氨水的目的是_________,此时所需pH的范围为_________,当调节溶液pH=5时,溶液中的c(Fe3+)=__________;
(4)反应3的离子方程式为__________,反应类型为__________;
(5)从滤液B中可回收的主要物质是__________;
(6)经检验分析,反应4 所得固体组成为Zna(OH)bCO3,称取该固体22.4g,焙烧后得固体16.2g,则a=_________。
查看答案和解析>>
科目:高中化学 来源:2017届贵州省贵阳市高三2月适应性考试(一)理综化学试卷(解析版) 题型:选择题
下列实验操作、现象和结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 向A12(SO4)3溶液中滴加过量氨水 | 溶液先浑浊后澄清 | Al(OH)3能溶于氨水 |
B | 将浓硫酸滴在胆矾晶体上 | 蓝色晶体变白 | 浓硫酸具有脱水性 |
C | 将新制的氯水滴在蓝色石蕊试纸上 | 试纸先变红后褪色 | Cl2有漂白性 |
D | 向某晶体的水溶液中加入2滴FeSO4溶液 | 产生特征蓝色沉淀 | 该晶体中一定含有[Fe(CN)6] 3- |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届河北省唐山市高三下学期第一次模拟考试理综化学试卷(解析版) 题型:选择题
地中海沿岸出产的一种贵重染料经化学分析,其主要组成的结构如图所示,下列说法不正确的是( )
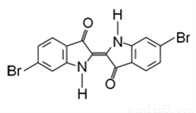
A. 属于烃的衍生物
B. 分子式为Cl6H8O2N2Br2
C. lmol该有机物与H2加成最多消耗9molH2
D. 该有机物溴元素检验可将有机物与碱液共热后,直接加入硝酸银溶液,观察是否有浅黄色沉淀生成
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二上学期期末考试化学试卷(解析版) 题型:填空题
H2SO4是工业上常用的酸,NH4Al(SO4)2是一种食品加工业中常用的食品添加剂,用于焙烤食品;NH4HSO4在分析试剂、医药、电子工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其原理是_____________(用离子方程式说明)。
(2)20℃时,均为0.1mol L-1的几种电解质溶液的pH 随温度变化的曲线如图1 所示。
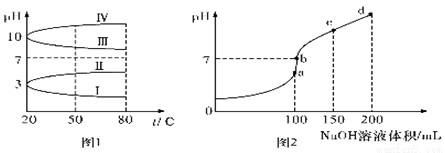
① 其中符合0.1mol·L-1 NH4Al(SO4)2溶液的pH随温度变化的曲线是_______(填罗马数字)。
② 20℃ 时,0.1mol·L-1NH4Al(SO4)2溶液中,2c(SO42-)-c(NH4+)-3c(Al3+)=____mol·L-1(填具体数字计算式,不必化简)
(3)室温时,向100mL0.1mol·L-1NH4HSO4溶液中滴加0.1mol L-1NaOH溶液,溶液pH 与NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d 四个点,水的电离程度最大的是__________点,在b点,溶液中各离子浓度由大到小的排列顺序是___________________。
(4)t℃ 时,pH=2的稀硫酸和pH=11的NaOH溶液等体积混合后溶液呈中性,则该温度下水的离子积常数Kw=________________。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省长沙市高二上学期期末考试化学试卷(解析版) 题型:选择题
下列关于热化学反应的描述中正确的是
A. HCl和NaOH反应的中和热△H=-57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热也是△H=-57.3kJ/mol
B. CO(g)的燃烧热是283.0kJ/mol,则2CO2(g)=2CO(g)+O2(g) △H=+566kJ/mol
C. 需要加热才能发生的反应一定是吸热反应
D. 1mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热
查看答案和解析>>
科目:高中化学 来源:2016-2017学年浙江省台州市高一上学期期末质量评估考试化学试卷(解析版) 题型:选择题
将某无色气体X通入品红溶液,溶液褪色;加热,溶液又变红色,X可能是
A. O2 B. Cl2 C. SO2 D. CO2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com