
完全燃烧2mol某有机物,可以收集到标准状况下89.6L的CO2和6mol的H2O,同时消耗6molO2,试推断该有机物的分子式是
A.C2H4 B.C2H4O C.C2H6 D.C2H6O
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
下列叙述正确的是()
| A. | 某物质中含有一种元素,则该物质一定是纯净物 | |
| B. | 金刚石和石墨之间的转变一定是化学变化 | |
| C. | 不同物质其相对分子质量一定不同 | |
| D. | 不同的原子可相互组合成复杂的原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
现有部分短周期元素的性质与原子(或分子)结构如下表:
| 元素编号 | 元素性质与原子(或分子)结构 |
| T | 最外层电子数是次外层电子数的3倍 |
| X | 常温下,单质为双原子分子,分子中含有3对共用电子对,其简单氢化物的水溶液显碱性 |
| Y | M层比K层少1个电子 |
| Z | 第3周期元素的简单离子中半径最小的,其氧化物呈两性 |
(1)画出元素T原子结构示意图__________________________;
(2)元素Y与元素Z相比,金属性较强的是______(用元素符号表示),下列表述中能证明这一事实的是____(填序号);
a.Y单质的熔点比Z单质低 b.Y的化合价比Z低
c.Y单质与水反应比Z单质剧烈 d.Y最高价氧化物的水化物的碱性比Z强
(3)T、X、Y、Z中有两种元素能形成既有离子键又有非极性共价键的化合物,写出该化合物的化学式为_______。
(4)元素T和氢元素以原子个数比1∶1形成的化合物的电子式为______,元素Z最高价氧化物的水化物与元素Y的最高价氧化物的水化物的溶液相互反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知2SO2+O2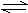 2SO3是一个正反应放热的可逆反应。如果反应在密闭容器中进行,则下列有关途述正确的是
2SO3是一个正反应放热的可逆反应。如果反应在密闭容器中进行,则下列有关途述正确的是
A.使用催化剂是为了加快反应 速率,提高生产效率
速率,提高生产效率
B.升高温度可加快逆反应速率但不能改变正反应速率
C.一定条件下,SO2可100%转化为SO3
D.任何条件下,反应达到平衡,SO2的浓度一定等于SO3的浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
下列金属冶炼的反应原理,错误的是
A.2 NaCl(熔融)
NaCl(熔融)  2Na+Cl2 B.Mg
2Na+Cl2 B.Mg O+H2
O+H2 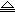 Mg+H2O
Mg+H2O
C .Fe3O4+4CO
.Fe3O4+4CO  3Fe+4CO2 D.2HgO
3Fe+4CO2 D.2HgO 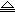 2Hg+O2
2Hg+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
“酒是陈的香”,就是因为酒在储存过程中生成了有香味的乙酸乙酯,在实验室我们也可以用下图所示的装置来制取乙酸乙酯。试回答下列问题:
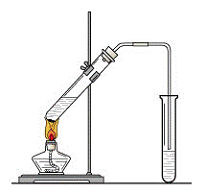 (1)写出由CH3COOH与C2H518OH制取乙酸乙酯的化学反应方程式 ;该反应属____反应。
(1)写出由CH3COOH与C2H518OH制取乙酸乙酯的化学反应方程式 ;该反应属____反应。
(2)该反应需加入一定量的浓硫酸,则浓硫酸的主要作用是 。
(3)装置中通蒸气的导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止 。
(4)若要把制得的乙酸乙酯分离出来,应采用的实验操作是 (填操作名称);主要使用的玻璃仪器是 。(答仪器的名称)
(5)生成乙酸乙酯的反应是可逆反应,反应物不能完全转化成生成物,反应一段时间后,达到了反应的限度,即达到化学平衡状态。下列描述能说明乙醇与乙酸的反应已 达到化学平衡状态的有(填序号) 。
达到化学平衡状态的有(填序号) 。
①单位时间里,生成1mol乙酸乙酯,同时生成1mol水
②单位时间里,生成1mol乙酸乙酯,同时生成1mol乙酸
③单位时间里,消耗1mol乙醇,同时消耗1mol乙酸
④正反应速率与逆反应速率相等
⑤反应混合物中各物质的浓度不再 变化
变化
查看答案和解析>>
科目:高中化学 来源: 题型:
烯烃A在一定条件下可以按下图进行:
已知:
CH3CH2CH2CH2CH2CH2Br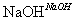 CH3CH2CH2CH2CH===CH2+HBr
CH3CH2CH2CH2CH===CH2+HBr
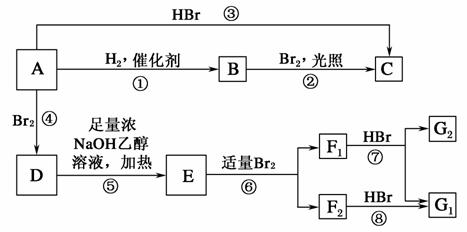
已知D为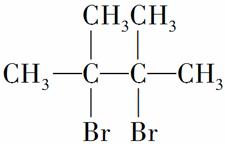 ,F1和F2互为同分异构体,G1和G2互为同分异构体。请填空:
,F1和F2互为同分异构体,G1和G2互为同分异构体。请填空:
(1)A的结构简式是:_________________________________ _______________________________________。
(2)框图中属于取代反应的是(填数字代号):________。
(3)框图中属于加成反应的是________。
(4)G1的结构简式是________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com