
| A. | CaCO3(s)═CaO(s)+CO2(g)在室温下不能自发进行,说明该反应的△H<0 | |
| B. | 焓变和熵变是判断反应方向的两个主要因素 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,反应速率v(H2)和H2的平衡转化率均增大 | |
| D. | 任何情况下,温度都不可能对反应的方向起决定性作用 |
分析 △H-T△S<0的反应可自发进行,且放热反应升高温度时平衡逆向移动,以此来解答.
解答 解:A.CaCO3(s)═CaO(s)+CO2(g)的△S>0,室温下不能自发进行,说明该反应的△H>0,故A错误;
B.由△H-T△S<0的反应可自发进行,则焓变和熵变是判断反应方向的两个主要因素,故B正确;
C.△H<0为放热反应,升高温度,反应速率加快,平衡逆向移动,则H2的平衡转化率减小,故C错误;
D.△H-T△S<0的反应可自发进行,△H>0、△S>0时温度对反应的方向起决定性作用,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握判断反应进行方向的综合判据、平衡影响因素为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Zn | B. | Fe | C. | Cu | D. | Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验室用液溴和苯在催化剂作用下制溴苯: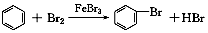 | |
| B. | 蛋壳溶于食醋:CaCO3+CH3COOH=CH3COOCa+H2O+CO2↑ | |
| C. | 甲醛溶液中加入足量新制碱性Cu(OH)2悬浊液并加热HCHO+2 Cu(OH)2+NaOH$\stackrel{△}{→}$ HCOONa+Cu2O↓+3H2O | |
| D. | 向氯乙烷水溶液中加入氢氧化钠溶液共热:CH3CH2Cl+NaOH $→_{△}^{水}$ CH2=CH2+NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 起始温度t1/℃ | 终止温度t2/℃ | 温度差 (t2-t1)/℃ | |||
| HCl | NaOH | 平均值 | |||
| 1 | 25.5 | 25.0 | 25.25 | 28.5 | 3.25 |
| 2 | 24.5 | 24.2 | 24.45 | 27.6 | 3.15 |
| 3 | 25.0 | 24.5 | 24.75 | 26.5 | 1.75 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4+、CO32-、Cl-、NO3- | B. | Pb2+、Fe3+、S2-、SO42- | ||
| C. | NH4+、H+、S2O32-、PO43- | D. | Ca2+、Al3+、Br-、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 当水结成冰时,水分子间的间距会减小,因而密度增大 | |
| B. | 玻璃态水与液态水具有不同酌化学性质 | |
| C. | 玻璃态水是水的一种特殊状态 | |
| D. | 纯净水与食盐水的冰点相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com