
����Ŀ��ʵ������Ҫ0.1 mol��L��1NaOH��Һ450 mL��0.5 mol��L��1������Һ500 mL��������������Һ����������ش��������⣺
(1)��ͼ��ʾ��������������Һ�϶�����Ҫ����________(�����)������������Һ�����õ��IJ���������________(����������)��

(2)���в����У�����ƿ�����߱��Ĺ�����________(�����)��
A������һ�����ȷŨ�ȵı���Һ B��������Һ
C����������ƿ������µ����������Һ�� D��ȷϡ��ijһŨ�ȵ���Һ
E�����������ܽ��������
(3)���ݼ�����������ƽ��ȡNaOH������Ϊ________g����ʵ����������������ȷ����NaOH��Һ��ת��������ƿʱδ����ȴ����������ҺŨ��________������ڡ������ڡ���С�ڡ���0.1 mol��L��1��
(4)���ݼ����֪��������������Ϊ98%���ܶ�Ϊ1.84 g��cm��3��Ũ��������Ϊ________mL(����������һλС��)��
���𰸡�AC���������ձ�BCE2.0����13.6
��������
��1�����Ʋ����м��㡢�������ܽ⡢��ȴ����Һ��ϴ�ӡ����ݡ�ҡ�ȵȲ�����һ����������ƽ��������ҩ��ȡ��ҩƷ�����ձ����ܽ⣨������Ͳ��ȡˮ������ȴ��ת�Ƶ�100mL����ƿ�У����ò���������������ˮ��Һ�����̶���1��2cmʱ�����ý�ͷ�ιܵμӣ�������Ҫ������Ϊ��������ƽ��ҩ�ס��ձ���Ͳ����������������ƿ����ͷ�ιܣ����Բ���Ҫ��������AC������Ҫ���������ձ��Ͳ��������ʴ�Ϊ��AC�����������ձ���
��2������ƿ�����������桢������Һ���ܽ�������ʵȣ�ֻ��1���̶��߲��ܲ�������ƿ������µ����������Һ�壬�ʴ�Ϊ��BCE��
��3��m=nM=CVM=0.1mol/L��0.5L��40g/mol=2g��������ƿ�ж���ʱ��������ƿ�̶��ߣ�������Һ�����ƫС������������Һ��Ũ��ƫ�ʴ�Ϊ��2.0�����ڣ�
��4��Ũ��������ʵ���Ũ��Ϊ��c=![]() =
=![]() mol/L=18.4mol/L������ҪŨ��������ΪV��0.5mol/L��0.5L=18.4mol/L��V��V=0.0136L=13.6mL���ʴ�Ϊ��13.6��
mol/L=18.4mol/L������ҪŨ��������ΪV��0.5mol/L��0.5L=18.4mol/L��V��V=0.0136L=13.6mL���ʴ�Ϊ��13.6��


 ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����״���£�VL�����ܽ���1Lˮ��(ˮ���ܶȽ���Ϊlg/mL)��������Һ���ܶ�Ϊ��g/mL����������Ϊ�أ�����Ũ��Ϊc mol/L�������й�ϵ�в���ȷ����
A. ��=![]() B. ��=
B. ��=![]() C. ��=
C. ��=![]() D.
D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������أ�K2FeO4����һ�ּ�������������������һ������Ͷ��ˮ���������������������£�
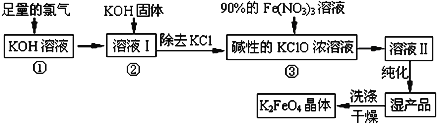
��֪����2KOH��Cl2��KCl��KClO��H2O���������¶Ƚϵͣ�
��6KOH��3Cl2 ��5KCl��KClO3��3H2O���������¶Ƚϸߣ�
�ش��������⣺
(1)����������Ӧ��______________�������¶Ƚϸ��������¶Ƚϵ�����������½��У�
(2)����ҺI�м���KOH�����Ŀ����________�����ţ���
A������ҺI�й�����Cl2������Ӧ�����ɸ����KClO
B��KOH�����ܽ�ʱ��ų��϶����������������߷�Ӧ����
C��Ϊ��һ����Ӧ�ṩ���ԵĻ���
D��ʹKClO3ת��Ϊ KClO
(3)����ҺII�з����K2FeO4�����и���ƷKNO3��KCl����Ӧ���з��������ӷ�Ӧ����ʽΪ________________________________________ ��
(4)����ж�K2FeO4�����Ѿ�ϴ�Ӹɾ�________________________________��
(5)������أ�K2FeO4����Ϊˮ��������һ���ŵ�������ˮ��Ӧ���ɽ����������ʣ���ƽ�÷�Ӧ�����ӷ���ʽ��_____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ȷ�������з�Ӧ�����ӷ���ʽΪ(����)
A. ��ϡ�����ȥˮ����2H����CaCO3===Ca2����CO2����H2O
B. ��������Ũ�����ϼ��ȣ�2H����FeS===H2S����Fe2��
C. ����������Һ�еμ�̼������Һ��2Al3����3CO32-===Al2(CO3)3��
D. Na2O2����ˮ����O2��Na2O2��H2O===2Na����2OH����O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ϩ������������Ҫ��ҽҩ�м��壬�㷺Ӧ���ںϳɸй���ϡ�����ϩ���������ͨ�����·�Ӧ�ϳɡ�
��Ӧ�٣�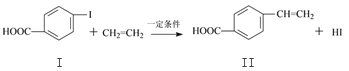
��1�����й��ڻ�����I�ͻ�������˵������ȷ����______________��
a��������I�������Ƶ�Cu��OH��2��Ӧ b�����ɷ���������Ӧ��������Ӧ
c�����������ʹKMnO4��Һ��ɫ d��1 mol��������������5 mol H2��Ӧ
��2����������ڴ������������ɸ߷��ӻ�����ķ�Ӧ����ʽΪ_____________��
��3�����������ɷ����廯�����ͨ����ȥ��Ӧ��ã����Cu���ȵIJ����ܷ���������Ӧ��д���������Ľṹ��ʽ__________________________��
��4����������ǻ�������ͬ���칹�壬�һ��������FeCl3��Һ����ɫ�������ϵ�һ�ȴ���ֻ��2�֣�д����������Ľṹ��ʽ________________________��дһ�֣���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���߷��Ӳ���PET������֬��PMMA�ĺϳ�·�����£�

��֪��  ��R��R�����������
��R��R�����������
��1���ٵķ�Ӧ������____________________��
��2���ڵĻ�ѧ����ʽΪ________________________________________��
��3��F�ĺ˴Ź���������ʾֻ��һ��壬�ݵĻ�ѧ����ʽΪ____________��
��4��G�Ľṹ��ʽΪ____________________��
��5���ߵĻ�ѧ����ʽΪ______________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ��ʹ�Ա�ڷɴ��еõ�һ���ȶ��ģ����õ����滷����һ���ڷɴ��ڰ�װʢ��Na2O2��K2O2������װ�ã�������;�Dz������������й���Na2O2��������ȷ���� (����)
A. Na2O2�����������ӵĸ�����Ϊ1��1
B. Na2O2�ֱ���ˮ��CO2��Ӧ������ͬ����O2ʱ����Ҫˮ��CO2���������
C. Na2O2�ֱ���ˮ��CO2��Ӧ������ͬ����O2ʱ��ת�Ƶ��ӵ����ʵ������
D. Na2O2��Ư��ԭ����SO2��Ư��ԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�����Һ�п��ܺ���HCl��MgCl2��AlCl3��NH4Cl��Na2CO3��KCl�еļ�������,������Һ����μ���NaOH��Һ,�������������ʵ���(n)������NaOH��Һ���(V)�Ĺ�ϵ��ͼ��ʾ���ش���������:
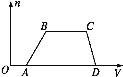
��1����Һ��һ�����е�������______________________(�ѧʽ)��
��2����Һ��һ�������е�������________________(�ѧʽ)��
��3����Һ�п��ܺ��е�������____(������),�жϸ������Ƿ���ڵ�ʵ�鷽����____,��������������_______________________________________________��
��4���ֱ�д��AB�Ρ�BC�η�����Ӧ�����ӷ���ʽ:
��AB��Ϊ_______________________________________________________________;
��BC��Ϊ_______________________________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������β��������̼��Ҫԭ��Ϊ2NO(g)+2CO(g)![]() N2(g)+2CO2(g) +Q��Q>0����һ���������ܱ�����
N2(g)+2CO2(g) +Q��Q>0����һ���������ܱ�����
�У��ô�������ø÷�Ӧ�ڲ�ͬʱ�� NO �� CO Ũ�����±���
ʱ��/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/molL-1 | 9.50��10-3 | 4.50��10-3 | 2.50��10-3 | 1.50��10-3 | 1.50��10-3 |
c(CO)/molL-1 | 9.00��10-3 | 4.00��10-3 | 2.00��10-3 | 1.00��10-3 | 1.00��10-3 |
���������գ�
��1�� д���÷�Ӧ��ƽ�ⳣ������ʽ��_________�� �¶����ߣ�������̼�����Ũ�Ƚ�______����������С�����䡱����
��2��ǰ 2s �ڵĵ�����ƽ����Ӧ�����ǣ�v(N2)=______mol/(Ls)���ﵽƽ��ʱ��CO ��ת����Ϊ��_____��
��3����ҵ�ϳ����á� ���³����������������� ������ͬʱ���� SO2 �͵������������壨NOx �����Ի��(NH4)2SO4 ��ϡ��Һ���ڴ���Һ�У�ˮ�ĵ���̶����ܵ���_____����ٽ����������ơ���û��Ӱ�족����
����(NH4)2SO4��Һ���ټ�������ϡ���ᣬ��![]() ֵ��_____����������С�����䡱����
ֵ��_____����������С�����䡱����
��4������� BaCl2 ��Һ��ͨ������ SO2 ���壬û�г������ɣ������μ�һ�����İ�ˮ��������ɰ�ɫ��������ƽ���ƶ�ԭ��������������___________________________��
��5������һ�ֿ����Ա�����Һ��ͨ������ SO2 ���壬������������ɫ�������ó����Ļ�ѧʽΪ_____�� ԭ�����Ա��ο�����_____��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com