
| A. | H2CrO4 | B. | H3PO4 | C. | H3AsO4 | D. | HBrO4 |
分析 含氧酸可用通式XOm(OH)n来表示,式中m大于等于2的是强酸,m为0的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强,将选项中含氧酸改写成XOm(OH)n形式,根据非羟基氧原子数目判断.
解答 解:含氧酸可用通式XOm(OH)n来表示,式中m大的是强酸,m小的是弱酸,据此可知,非羟基氧原子数目越大,酸性越强,
A.H2CrO4可以改写为CrO2(OH)2,非羟基氧原子数目为2;
B.H3PO4可以改写为PO1(OH)3,非羟基氧原子数目为1;
C.H3AsO4可以改写为AsO1(OH)3,非羟基氧原子数目为1;
D.HBrO4可以改写为BrO3(OH)1,非羟基氧原子数目为3;
HBrO4中非羟基氧原子数目最多,酸性最强,
故选D.
点评 本题考查了含氧酸酸性强弱的判断方法,主要考查学生阅读获取信息的能力,题目难度不大,读懂信息是解题的关键.


科目:高中化学 来源: 题型:选择题
| A. | ②④⑤ | B. | ①③④ | C. | ①②③④ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LN2和NH3混合气体中原子间共有3NA个共用电子对 | |
| B. | 共NA个一氧化二氮和二氧化碳分子的混合气体的质量是44克 | |
| C. | 25℃时pH=1的醋酸溶液中含有H+的数目为0.1NA | |
| D. | 标准状况下,2.24L SO3含有的分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,该元素的名称是氧;
,该元素的名称是氧;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝热反应属于氧化还原反应,且生成物的总能量高于反应物的总能量 | |
| B. | 在相同温度和压强下,等质量的硫在足量的纯氧中燃烧放出能量为 Q1,在空气中燃烧放出能量为 Q2,则 Q1=Q2 | |
| C. | 需要加热的反应一定是吸热反应 | |
| D. | 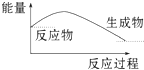 Ba(OH)2•8H2O 晶体和 NH4Cl 晶体反应能量变化如图所示 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图为实验室某浓盐酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶的标签,试根据标签上的有关数据回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,结构简式H2C=CH2.
,结构简式H2C=CH2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com