
科目:高中化学 来源: 题型:解答题

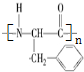 (写结构简式);
(写结构简式); ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:
甲是一种可用于净水和膨化食品的盐,由A、B、C、D、E五种短周期元素组成.甲溶于水后可电离出三种离子,其中一种是由A、B形成的10电子阳离子.A元素原子核内质子数比E的少l,D、E同主族.某同学为探究甲的组成而进行如下实验:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
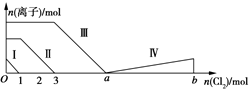 向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法正确的是( )
向含Fe2+、I-、Br-的溶液中通入过量的氯气,溶液中四种粒子的物质的量变化如图所示,已知b-a=5线段Ⅳ表示一种含氧酸,且Ⅰ和Ⅳ表示的物质中含有相同的元素.下列说法正确的是( )| A. | 线段Ⅱ表示Br-的变化情况 | B. | 原溶液中n(FeI2):n(FeBr2)=3:1 | ||
| C. | 根据图象无法计算a的值 | D. | 线段Ⅳ表示IO${\;}_{3}^{-}$的变化情况 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在碱性溶液中:Na+、NH4-、Cl-、NO3- | |
| B. | pH=4的无色溶液中:Na+、Ba2+、Cl-、SO32- | |
| C. | pH=10的无色溶液中:H+、NH4-、HCO3-、Cl- | |
| D. | 中性溶液中:K+、Na+、NO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图为美国布朗大学的科学家使用硅碲化物制造出的新型纳米颗粒材料,可广泛应用于电子和光学设备中.将该纳米颗粒分散到水中,下列有关该分散系的说法中正确的是( )
如图为美国布朗大学的科学家使用硅碲化物制造出的新型纳米颗粒材料,可广泛应用于电子和光学设备中.将该纳米颗粒分散到水中,下列有关该分散系的说法中正确的是( )| A. | 该分散系属于溶液 | B. | 该分散系能产生丁达尔效应 | ||
| C. | 该分散系不能通过滤纸 | D. | 该分散系的隐定性强于食盐水 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na和O2 | B. | Fe和稀HNO3 | C. | Cu和FeCl3溶液 | D. | Na2CO3和稀HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com