
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 0.01mol?L-1KIO3酸性溶液(含淀粉)的体积/mL | 0.01mol?L-1Na2SO3溶液的体积/mL | H2O的体积/mL | 实验温度 /℃ |
溶液出现蓝色时所需时间/s | |
| 实验1 | 5 | V1 | 35 | 25 | |
| 实验2 | 5 | 5 | 40 | 25 | |
| 实验3 | 5 | 5 | V2 | 0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.完成下列各题:
乙炔是一种重要的有机化工原料,以乙炔为原料在不同的反应条件下可以转化成以下化合物.完成下列各题:查看答案和解析>>
科目:高中化学 来源: 题型:
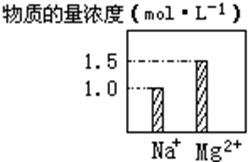 在0.2L NaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,回答下列问题:
在0.2L NaCl、MgCl2的混合溶液中,部分离子浓度大小如图所示,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、一定有乙烯 |
| B、一定有甲烷 |
| C、可能有丙烯 |
| D、可能有乙烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、盐酸、水煤气、硫酸、醋酸、干冰 |
| B、聚氯乙烯、漂白粉、苛性钠、硫化氢、氯气 |
| C、冰醋酸、碘酒、硫酸钡、氨水、一氧化碳 |
| D、冰水混合物、胆矾、氯化钾、次氯酸、乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、上述生成Ni(CO)4(g)的反应为吸热反应 |
| B、80℃时,测得某时刻Ni(CO)4、CO的浓度均为0.5 mol?L-1,则此时v (正)<v (逆) |
| C、恒温恒压下,向容器中再充入少量的Ar,上述平衡将正向移动 |
| D、恒温恒容下,向容器中再充入少量Ni(CO)4(g),达新平衡时,CO的浓度将增大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com