
| A. | 比较去锈的铁钉和去锈的绕有细铜丝的铁钉与同浓度的盐酸反应速率快慢时,可以加K3[Fe(CN)6]溶液,观察铁钉周围出现蓝色沉淀的快慢 | |
| B. | 将在空气中灼烧呈黑色的铜丝趁热插入盛有乙醇的试管中,铜丝变红色;反复数次,试管中的液体出现刺激性气味,表明乙醇已被铜氧化为乙醛 | |
| C. | 欲粗略测定某未知浓度的醋酸溶液中醋酸的电离常数Ka,应做的实验和所需的试剂(或试纸)为:中和滴定实验、pH试纸 | |
| D. | 从海带中提取碘,可将灰化后的海带加入水中煮沸一段时间后过滤,向滤液中滴入几滴硫酸,再加入适量H2O2溶液氧化,最后加入CCl4萃取分离 |
分析 A、亚铁离子和铁氰化钾溶液反应生成蓝色沉淀;
B、Cu与氧气反应生成CuO,CuO与乙醇反应生成乙醛;
C、确定醋酸的电离常数,根据CH3COOH?CH3COO-+H+,应分别确定CH3COOH的物质的量浓度和H+的物质的量浓度,可用滴定法确定CH3COOH的物质的量浓度,用pH试纸可粗略确定H+的物质的量浓度;
D、海带中含有碘离子,在酸性环境中过氧化氢能够氧化碘离子,碘单质易溶于有机溶剂.
解答 解:A、去锈的绕有细铜丝的铁钉在盐酸溶液中形成原电池,产生亚铁离子速度快,与铁氰化钾溶液反应生成蓝色沉淀所用的时间短,故A正确;
B、Cu与氧气反应生成CuO,CuO与乙醇反应生成乙醛,不是乙醇被铜氧化,故B错误;
C、可用滴定法确定CH3COOH的物质的量浓度,用pH试纸可粗略确定H+的物质的量浓度,进而计算电离常数,故C正确;
D、海带中含有碘离子,在酸性环境中过氧化氢能够氧化碘离子,碘单质易溶于CCl4,最后加入CCl4萃取分离,故D正确;
故选B.
点评 本题考查了物质性质和离子检验的实验操作,题目难度较大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
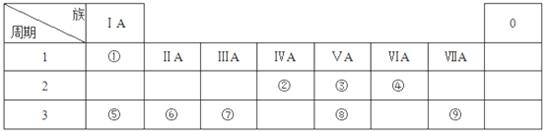
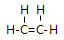 ;由④和⑥两种元素组成的化合物的电子式为
;由④和⑥两种元素组成的化合物的电子式为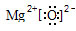 ;元素⑨的原子结构示意图为
;元素⑨的原子结构示意图为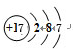 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
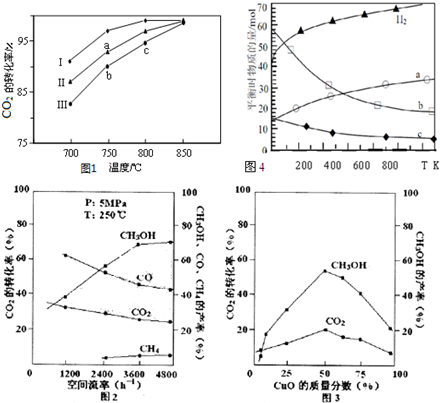
| 催化剂组分质量分数(%) | CuO | 0 | 25 | 50 | 75 | 100 |
| ZnO | 100 | 75 | 50 | 25 | 0 | |
| 到达平衡所需时间(h) | 2.5 | 7.4 | 8.1 | 12 | 无催化活性 | |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
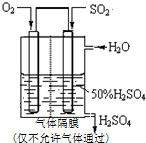 已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ•mol-1.
已知:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g)△H=-98kJ•mol-1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 汽油、柴油和植物油都是碳氢化合物 | |
| B. | 葡萄糖和银氨溶液发生银镜反应可用作制镜子 | |
| C. | 往花生油中加入稀硫酸能发生皂化反应 | |
| D. | 鸡蛋清中加入胆矾可以使蛋白质发生盐析 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向硫酸铜溶液中加入NaHS溶液:Cu2++HS-=CuS↓+H+ | |
| B. | 用醋酸除去水垢中的碳酸钙:CaCO3+2H+=Ca2++H2O+CO2↑ | |
| C. | 用强碱溶液吸收工业制取硝酸尾气:NO+NO2+2OH-=2NO3-+H2O | |
| D. | 将少量SO2气体通入氨水中:SO2+NH3•H2O=NH4++HSO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将浓硫酸和浓硝酸分别长期露置在空气中,浓度均会降低 | |
| B. | 在常温下,浓硫酸和浓硝酸均能与铜剧烈反应 | |
| C. | 稀硫酸和稀硝酸分别与金属反应时,S和N元素的化合价都会发生变化 | |
| D. | 因为浓硫酸和浓硝酸都能与铁反应,所以常温下二者都不能用铁制容器盛装 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com