
A��B��D��E��G��M����Ԫ��λ��Ԫ�����ڱ�ǰ�����ڣ�ԭ�����������������У�Ԫ��A��һ�ֺ��������ӣ�B�ĵ��ʼ��з��Ӿ�������ԭ�Ӿ��壬������DE2Ϊ����ɫ���壬G��ǰ�������е縺����С��Ԫ�أ�M��ԭ�Ӻ����������G��10��
��ش��������⣺
��1����̬Gԭ�ӵĺ�������Ų�ʽ��________��M��Ԫ�����ڱ��е�λ����_______��Ԫ��B��D��E�ĵ�һ�������ɴ�С��˳��Ϊ______________����Ԫ�ط��ű�ʾ����
��2��Ԫ��A��E��ɵ������ӿռ乹��Ϊ________��������ABD�ĽṹʽΪ______������Bԭ�ӵ��ӻ���ʽΪ________��
<span style="font-size: 15px; font-family: "����";"><span contenteditable="true">��3��</span></span>D������������Ӧ��ˮ�����������DA3�����������ӻ������ң������£����ס�������Һ��pH������5������ˮ������� =_________������Һ���������ӵ����ʵ���Ũ���ɴ�С��˳����_______________________________��
=_________������Һ���������ӵ����ʵ���Ũ���ɴ�С��˳����_______________________________��
��4��Ԫ��Xλ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ2��Ԫ��Y��̬ԭ�ӵ�3p�������4�����ӡ�
��X��Y���γɻ�������X�Ļ��ϼ۵�������������Y�ﵽ8���ӵ��ȶ��ṹ��û�����Ļ�ѧʽΪ______________��
��E���⻯�H2E�����Ҵ��е��ܽ�ȴ���H2Y����ԭ����_________________��
��X���Ȼ����백ˮ��Ӧ���γ������[X(NH3)4]Cl2��1mol��������к��Ц� ������ĿΪ___________��
 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ�����и�һ��ѧ�ڿ�ѧ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
A��B��C��D��E �Ǻ˵����������������ֶ�����Ԫ�أ�ԭ�Ӱ뾶��D��E��B��C��A˳�����μ�С��B��Eͬ���壬�����ƶϲ���ȷ����
A. A��B��Eһ���ڲ�ͬ����
B. A��D������ͬһ����
C. C��D�ĵ��ʿ��ܻ����γ����ӻ�����
D. C������������ˮ��������Լ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʦ����ѧ������ѧ��һ3���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
���и�������������ͬλ�ص���(����)
A. 16O��18O B. H2O��D2O C. H2��D2 D. 24Mg��24Na
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ�����и�����ѧ�ڵ�һ������������ۻ�ѧ�Ծ��������棩 ���ͣ������
���̿����Ҫ�ɷ���MnO2��������Һ������������SO2���������Խ���Һ�ֿ������Ʊ��ߴ������̣���һ�ֹ�����������ͼ��ʾ���ش��������⣺
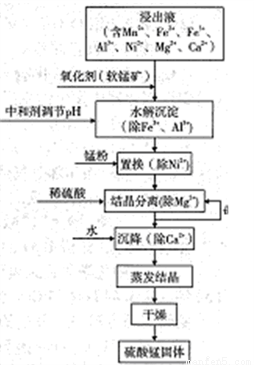
(1)���̿�����Һ����SO2�Ĺ����У�SO2������________�ԡ�
(2)����������������Ӧ�����ӷ���ʽΪ____________��
(3)��֪��Ksp[Al(OH) 3]=1.0��10-34��
Krp[Fe(OH) 3]=2.6��10-30��
Krp[Ni(OH) 2]=1.6��10-15��
Krp[Mn(OH) 2]=4.0��10-14��
��ˮ��������У�
�١��кͼ���������________�����ţ�
A.Al2O3 B.H2SO4 C.MgO D.MnO2
����Һ��pHӦ������________������Ũ��С��1��10-5mol��L-1ʱ��������Ϊ�����ӳ�����ȫ��
�۲����á�ˮ���������Ni2+��ԭ����___________��
(4)���û����з�����Ӧ�����ӷ���ʽΪ____________��
(5)����Ʒ���롱�еIJ������ʵ��ܽ����������ͼ��
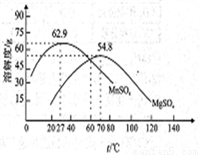
�ټ���ϡ����������ǣ����ƽ���ƶ�ԭ�����ͣ�_____________��
�ڽᾧ����˹����У���ϵ�¶Ⱦ�Ӧά����_______�棨�27������60����70������
(6)�ߴ������̿�����ˮ���ܽ��������IJⶨ���������£�
����1��ˮ�е������ڼ�����Һ�н�MnSO4����ΪMnO(OH)2��
����2�������������£�����KI�����ɵ�MnO(OH)2�ٻ�ԭ��Mn2+��
����3����Na2S2O3����Һ�ζ�����2�����ɵ�I2(2S2O32-+I2=2I-+S4O62-)��
ȡijˮ��100mL���������ⶨ����ζ�������a mol��L-1 NaS2O3����ҺVmL����ˮ���ܽ�������Ϊ
_________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�츣��ʡ�����и�����ѧ�ڵ�һ������������ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӏ�������ֵ�������й�������ȷ����
A. .25��ʱ��1LpH =11�İ�ˮ��OH-Ϊ0.001 NA
B. ��״���£�2.24 L SO3����ԭ����Ϊ0.3NA
C. 4.6 g�Ҵ��к��еĹ��ۼ���Ϊ0. 7NA
D. 3.6gD2O����������Ϊ2NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�ɶ������и߶���ѧ����ĩ��⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�����йط���ʽ��д��ȷ���ǣ� ��
A��������Һ������������Һ��Ӧ�����ӷ���ʽΪH����OH����H2O
B��H2S��ˮ��Һ�еĵ��룺H2S+H2O H3O++ HS��
H3O++ HS��
C�������ȼ����Ϊ890.3 kJ��mol��1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��
CH4 (g)��2O2 (g) == CO2 (g)��2H2O (g) ��H����890.3 kJ��mol��1
D��˫��ˮ�м���ϡ�����KI��Һ: H2O2+ 2I-+H+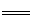 I2+ 2H2O
I2+ 2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���Ĵ�ʡ�ɶ������и߶���ѧ����ĩ��⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͼ��ʾ�������ݻ���ͬ�������٢ڢ��н������·�Ӧ��3A(g)��B(g) 2C(g) ��H<0������ʼ�¶���ͬ���ֱ�������������ͨ��3molA��1molB����ﵽƽ��ʱ��������C���ʵ���������ɴ�С��˳��Ϊ �� ��
2C(g) ��H<0������ʼ�¶���ͬ���ֱ�������������ͨ��3molA��1molB����ﵽƽ��ʱ��������C���ʵ���������ɴ�С��˳��Ϊ �� ��
A���ۢڢ� B���ۢ٢� C���٢ڢ� D���ڢ٢�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��ɽ��ʡ2016-2017ѧ���һ3���¿���ѧ�Ծ� ���ͣ�ѡ����
X��Y��Z���ֶ�����Ԫ�أ�ԭ�Ӱ뾶�Ĵ�С��ϵΪ��r(y)>r(x)>r(z)��ԭ������֮��Ϊ16��X��Y��Z����Ԫ�صij����������ʵ������¿ɷ�����ͼ��ʾ�仯������B��C��Ϊ10���ӷ��ӡ�����˵������ȷ����
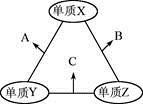
A. XԪ��λ�ڢ�A
B. A�����ܽ���B��
C. B�ķе����C�ķе�
D. A��C�����ܷ���������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2017�콭��ʡ�Ͼ��С��γ��и����ڶ���ģ�⿼�Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
����ϩ��һ����Ҫ�Ļ���ԭ�ϣ�ʵ���ҳ������з�Ӧ�Ʊ�����ϩ��
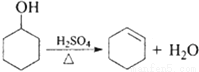
������������ϩ�IJ����������ʼ��±���
���� | �е㣨�棩 | �ܶȣ�g��cm-3��20�棩 | �ܽ��� |
������ | 161.1(97.8)* | 0.9624 | ������ˮ |
����ϩ | 83(70.8)* | 0.8085 | ������ˮ |
*�����е����ݱ�ʾ���л�����ˮ�γɵľ��й̶���ɵĻ�������л������������
���Ʊ�����ϩ��Ʒ��ʵ���н���������Ũ�����ϼ�����ƿ�У���ͼ��ʾװ�ã���ԡ���ȣ�����Լ1h���ռ���֣��õ���Ҫ������ϩ��ˮ�Ļ���
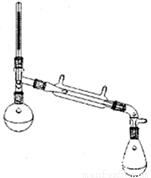
����ϩ���ᴿ����Ҫ�����У�
a.�����Һ�м��뾫�������ͣ�
b.����3��4mL5%Na2CO3��Һ��
c.���ã���Һ��
d.������ˮCaCl2���壻
e.����
�ش��������⣺
(1)��ԡ���ȹ����У��¶ȿ�����90�����£������¶Ȳ��˹��ߵ�ԭ����________��
(2)�����ܳ����뻷��ϩ��ˮ��ԭ����_______________��
(3)���뾫�������͵�Ŀ����_____________________��
(4)����3��4mL5%Na2CO3��Һ��������__________��
(5)������ˮCaCl2�����������______________��
(6)���ú˴Ź��������Լ����Ʊ��IJ����Ƿ�Ϊ����ϩ������ϩ��������_______�ֲ�ͬ��������ԭ�ӡ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com