
【题目】下列化学方程式中,正确的是( )
A.甲烷的燃烧热△H=﹣890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=﹣890.3kJ/mol
B.一定条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热akJ,其热化学方程式为:N2(g)+3H2(g)2NH3(g)△H=﹣2akJ/mol
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJ/mol
D.HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热△H=﹣114.6kJ/mol
【答案】C
【解析】解:A.甲烷的燃烧热△H=﹣890.3kJ/mol,燃烧热中生成水的状态应该为液态,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=﹣890.3kJ/mol,故A错误;B.一定条件下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热akJ,该反应为可逆反应,生成氨气的物质的量小于1mol,则生成2mol氨气放出的热量大于2akJ,正确的热化学方程式为:N2(g)+3H2(g)2NH3(g)△H<﹣2akJ/mol,故B错误;
C.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,2g氢气的物质的量为: ![]() =1mol,则2mol氢气燃烧生成液态水放出的热量为:285.8kJ×2=571.6kJ,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJ/mol,故C正确;
=1mol,则2mol氢气燃烧生成液态水放出的热量为:285.8kJ×2=571.6kJ,氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=﹣571.6kJ/mol,故C正确;
D.HCl和NaOH反应的中和热△H=﹣57.3kJ/mol,则H2SO4和Ba(OH)2反应的中和热仍然为△H=﹣57.3kJ/mol,由于硫酸与氢氧化钡还生成硫酸钡沉淀,放热热量增大,则硫酸与氢氧化钡反应的△H<﹣114.6kJ/mol,故D错误;
故选C.


 夺冠金卷全能练考系列答案
夺冠金卷全能练考系列答案科目:高中化学 来源: 题型:
【题目】下列说法不正确的是 ( )
A.微热可以促使亚甲基蓝变为亚甲基白
B.微热可以促使亚甲基白变为亚甲基蓝
C.碱性条件下,亚甲基蓝易变为亚甲基白
D.酸性条件下,亚甲基蓝易变为亚甲基白
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,在3支相同体积的试管中分别充有体积比为4:1的2种混合的气体,它们是: ①NO和NO2②NO2和O2③NH3和N2,现将3支试管均倒置于水槽中,充分反应后,试管中溶液物质的量浓度之比为
A. 1:1:1 B. 5:4:4 C. 4:4:5 D. 5:4:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.某工厂的工业废水中含有大量的FeSO4和较多的Fe3+和Cu2+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。实验室模拟该工业流程如图:
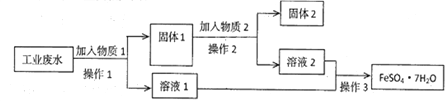
(1)检验废水中的Fe2+,实验室中用酸性KMnO4溶液检验,发生反应的离子方程式为________________________。
(2)加入过量物质1后,发生反应的离子方程式为___________________________。
(3)固体2是_____________________,实验室为长期保存硫酸亚铁溶液往往向其溶液中加入_______________________。
Ⅱ.工业上冶炼铝的原料是铝土矿(主要成分是Al2O3,杂质为Fe2O3、FeO、SiO2等)。某研究小组设计的提纯Al2O3的方案如下:

(1)加入过量的NaOH溶液,过滤后的滤液中含有的溶质有________(填化学式)。
(2)加入过量NaOH溶液过滤后,若滤渣中Fe(OH)2也被氧化,写出其被氧化的化学方程式__________________________。
(3)写出通入过量CO2生成沉淀A时反应的离子方程式为_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学﹣﹣选修5有机化学基础]I.已知有机物A仅含碳、氢、氧3种元素,质谱分析可知其相对分子质量为46,核磁共 振氢谱显示分子中有三种不同化学环境的氢原子,且有如下的转化关系: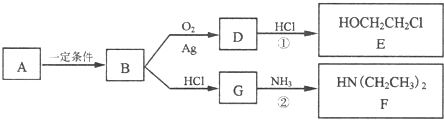
(1)由A→B的反应类型是
(2)D的红外光谱表明分子内除C一H键、C一C键外还含有两个C一O单键,反应①中 D与HCl按物质的量之比1:1反应,则D的结构简式是II.化合物E和F是药品普鲁卡因合成的重要原料,普鲁卡因的合成路线如下:已知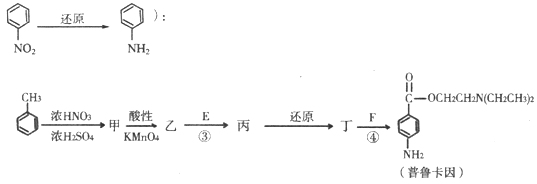
(3)丁的结构简式为
(4)反应③的化学方程式是
(5)普鲁卡因有两种水解产物戊和己,且戊与甲具有相同的分子式.符合下列条件的戊的同分异构体有种(包含戊);a.分子结构中含苯环,且每个苯环有2个侧链
b.分子结构中一定含官能团一NH2且一NH2直接与碳原子相连
(6)戊经聚合反应制成的高分子纤维广泛用于通讯、宇航等领域.该聚合反应的化学方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于0.1mol/L H2SO4溶液的叙述错误的是( )
A.1L该溶液中含有H2SO4的质量为9.8g
B.0.5L该溶液中氢离子的物质的量浓度为0.2mol/L
C.从1L该溶液中取出100mL,则取出溶液中H2SO4的物质的量浓度为0.01mol/L
D.取该溶液10mL,加水稀释至100mL后H2SO4的物质的量浓度为0.01mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下,CO和CH4燃烧的热化学方程式分别为:
2CO(g)+O2(g)═2CO2(g)△H=﹣566kJmol﹣1
CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H=﹣890kJmol﹣1
由1mol CO和3mol CH4组成的混合气体在该条件下完全燃烧释放的热量为( )
A.2912 kJ
B.3236 kJ
C.2953 kJ
D.3867 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锡、铅两种元素的主要化合价是+2价和+4价,其中+2价锡元素和+4价铅元素的化合物均是不稳定的,+2价锡元素有强还原性,+4价铅元素的化合物有强氧化性,例如:Sn2+还原性比Fe2+还原性强,PbO2的氧化性比Cl2的氧化性强,根据以上的叙述,回答有关的问题:
(1)写出下列反应的化学方程式:
①氯气与锡共热______________; ②氯气与铅共热______________;
③PbO2与浓盐酸共热_________________。
(2)能说明Sn2+还原性比Fe2+还原性强的离子方程式为________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com