
【题目】在下列物质中加入少量水,不能发生放出热量的化学反应的有( )
A.钠B.过氧化钠C.氧化钙D.碳酸氢钠
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:
【题目】下列有关物质结构和性质的说法不正确的是
A. 分子式为C5H10且与乙烯互为同系物的结构共有5种
B. 可用燃烧法鉴别环乙烷、苯、CCl4
C. 分子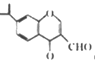 中所有碳原子不可能位于同一平面
中所有碳原子不可能位于同一平面
D. 三联苯![]() 与四联苯
与四联苯![]() 互为同系物
互为同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以食盐为原料进行生产并综合利用的某些过程如图。
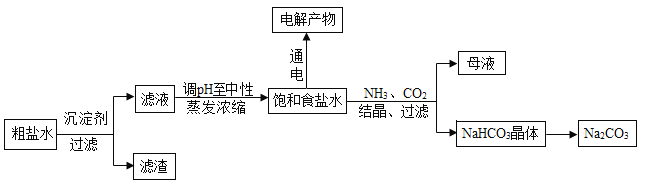
(1) 除去粗盐中的微溶物质CaSO4通常用Na2CO3处理,请用平衡移动原理解释说明:_____________。
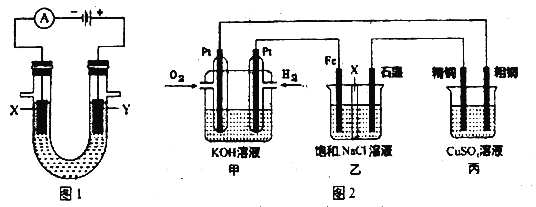
(2) 人们习惯上把电解饱和食盐水的工业叫做氯碱工业.图1表示电解饱和NaCl 溶液的装置,X、Y是石墨棒。实验开始后,检验Y 电极反应产物的方法是_________________。
(3) 若向分离出NaHCO3晶体后的母液中加入过量生石灰,则可获得一种可以循环使用的气体,其化学式是__________。
(4) 某同学设计一个燃料电池(如图2所示),目的是探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X 为阳离子交换膜。根据要求回答相关问题:
①通入氢气电极的反应式为__________________。
②反应一段时间后,在乙装置中滴入酚酞溶液,______________(填“铁”或“石墨”)极区的溶液先变红。
③如果粗铜中含有锌、银等杂质,丙装置中反应一段时间后,硫酸铜溶液浓度将___________(填“增大”“减小”或“不变”)。
④若在标准状况下有224mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ:乙烯产量是衡量一个国家石油化工水平的主要标志。下图是由乙烯合成乙酸乙酯可能的合成路线:
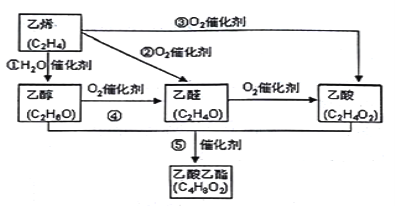
请回答下列问题:
(1)反应④的化学方程式为_____________________________ ;
(2)在实验室制备乙酸乙酯时,用到饱和的碳酸钠溶液,其作用是:___________________;
(3)乙醇的结构式为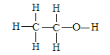 ,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 _________________________________;
,若实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 _________________________________;
Ⅱ:酸奶中含有乳酸,乳酸在常温常压下是一种无色的粘度很大的液体。取9.0g乳酸与足量的Na反应,在标准状况下可收集到2.24L气体;另取9.0g乳酸与足量的NaHCO3溶液反应,生成的CO2气体在标准状况下体积为2.24L。已知乳酸分子中含有一个甲基,请回答下列问题:
(1)乳酸的相对分子质量为:_______________________;
(2)在浓硫酸存在的条件下,两分子乳酸相互反应生成环状酯类化合物,请写出该反应的化学反应方程式:________________________,其反应类型为:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物A经李比希法和质谱法分析得知其相对分子质量为136,分子式为C8H8O2。A的核磁共振氢谱有4个峰且面积之比为1:2:2:3,A分子中只含一个苯环且苯环上只有一个取代基,其红外光谱与核磁共振氢谱如下图。关于A的下列说法中,正确的是( )
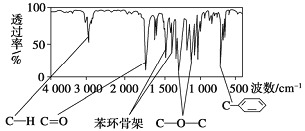

A. 与A属于同类化合物的同分异构体只有2种
B. A在一定条件下可与4molH2发生加成反应
C. A分子属于酯类化合物,在一定条件下不能发生水解反应
D. 符合题中A分子结构特征的有机物只有1种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是
A. 1mol 的P4O6中含有6 NA个P—O键
B. 0.1mo1H2和0.1molI2于密闭容器中充分反应后,分子总数小于0.2 NA
C. pH=3的CH3COOH溶液中,含有10-3NA个H+
D. 高温下,16.8gFe 与足量的水蒸气反应,失去0.8NA个电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列涉及化学学科观点的有关说法正确的是![]()
A. 微粒观:二氧化硫是由硫原子和氧原子构成的
B. 转化观:升高温度可以将不饱和硝酸钾溶液转变为饱和
C. 守恒观:1g镁与1g稀硫酸充分反应后所得的溶液质量为2g
D. 结构观:金刚石和石墨由于结构中碳原子的排列方式不同,性质存在着较大的差异
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、乙酸乙酯是重要的有机合成中间体,广泛应用于化学工业。实验室利用如图的装置制备乙酸乙酯。
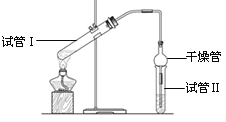
(1)与教材采用的实验装置不同,此装置中采用了球形干燥管,其作用是:_____________。
(2)请写出用CH3CH218OH制备乙酸乙酯的化学方程式:_____________,反应类型为_______。
(3)为了证明浓硫酸在该反应中起到了催化剂和吸水剂的作用,某同学利用上图所示装置进行了以下4个实验。实验开始先用酒精灯微热3min,再加热使之微微沸腾3min。实验结束后充分振荡小试管Ⅱ再测有机层的厚度,实验记录如下:
实验 编号 | 试管Ⅰ中的试剂 | 试管Ⅱ中的试剂 | 有机层的厚度/cm |
A | 2 mL乙醇、1 mL乙酸、 1mL18mol·L-1 浓硫酸 | 饱和Na2CO3溶液 | 3.0 |
B | 2 mL乙醇、1 mL乙酸 | 0.1 | |
C | 2 mL乙醇、1 mL乙酸、 3 mL 2mol·L-1 H2SO4 | 0.6 | |
D | 2 mL乙醇、1 mL乙酸、盐酸 | 0.6 |
①实验D的目的是与实验C相对照,证明H+对酯化反应具有催化作用。实验D中应加入盐酸的体积和浓度分别是______mL和_____mol·L-1 。
②分析实验_________________(填实验编号)的数据,可以推测出浓H2SO4的吸水性提高了乙酸乙酯的产率。
(4)若现有乙酸90g,乙醇138g发生酯化反应得到80g乙酸乙酯,试计算该反应的产率为______________(用百分数表示,保留一位小数)。
II、已知乳酸的结构简式为![]() 。试回答:
。试回答:
①乳酸分子中的官能团有:_____________________________________(写名称);
②乳酸与足量金属钠反应的化学方程式为________________________________;
③已知—COOH不会发生催化氧化,写出加热时,乳酸在Cu作用下与O2反应的化学方程式:________________________________________________;
④腈纶织物产泛地用作衣物、床上用品等。腈纶是由CH2=CH-CN聚合而成的。 写出在催化剂、加热条件下制备腈纶的化学方程式________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com