
| A. | 因为河虾中含有砷元素,所以不能食用 | |
| B. | “两者同食”发生的反应中维生素C作氧化剂 | |
| C. | 五价砷在维生素C作用下发生了还原反应 | |
| D. | 已知砒霜的主要成分是氧化砷,可以推测所含的砷元素化合价为+5 |
分析 A、五价砷是无毒的,三价砷有毒;
B、氧化剂在反应中发生还原反应;
C、根据维生素C的作用:将五价砷转化为三价砷来回答;
D、五价砷是无毒的,三价砷有毒,砒霜的毒性即为砷元素的毒性.
解答 解:A、河虾中含有砷元素为五价砷,是无毒的,能食用,三价砷有毒,故A错误;
B、根据维生素C的作用是将五价砷转化为三价砷,所以五价砷做氧化剂,维生素C做还原剂,五价砷发生了还原反应,故B错误;
C、由信息可知,反应中砷元素的化合价降低,则维生素C中某元素的化合价升高,则维生素C在反应中作还原剂,所以五价砷发生了还原反应,故C正确;
D、五价砷是无毒的,三价砷有毒,砒霜的毒性即为砷元素的毒性,砒霜中所含的砷元素化合价为+3,故D错误.
故选C.
点评 本题以生活中的信息来考查氧化还原反应,明确信息中砷元素的化合价变化是解答本题的关键,信息的获取和应用是解答本题的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 反应物能量总和大于生成物能量总和 | |
| B. | 反应中生成1mol水蒸气放出285.8 kJ的热量 | |
| C. | 2H2O(1)=2H2(g)+O2(g)△H=+571.6 kJ.mol-1 | |
| D. | 当反应中有2 mol H-H键断裂,该反应放出571.6 kJ的热量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,11.2L氯气所含原子数目为NA | |
| B. | 3mol单质Fe完全转变为Fe3O4,失去8NA个电子 | |
| C. | 标准状况下,11.2L SO3 中含有2NA个原子 | |
| D. | 用石灰乳完全吸收1 mol Cl2时,转移电子的数目是2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

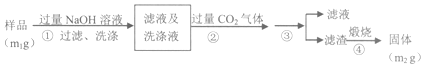
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝不易发生化学反应 | |
| B. | 铝的氧化物易发生还原反应 | |
| C. | 铝不易被氧化 | |
| D. | 铝易被氧化为氧化铝,氧化铝膜具有保护内部铝的作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 用玻璃棒蘸取浓硝酸点到蓝色石蕊试纸上 | 试纸先变红色后褪色 | 浓硝酸有酸性和氧化性 |
| B | CO2通入BaCl2溶液中 | 有白色沉淀出现 | 生成了BaCO3沉淀 |
| C | Al箔插入稀HNO3中 | 无现象 | Al箔表面被HNO3氧化,形成致密的氧化膜 |
| D | 过量的Fe粉中加入HNO3,充分反应后,滴入KSCN溶液 | 溶液呈红色 | 稀HNO3将Fe氧化为Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
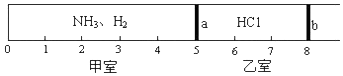
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a>b>c>d | B. | a>c>d>b | C. | c>a>b>d | D. | b>d>c>a |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com