
【题目】下列有关化学键的描述说法正确的是( )
①水分子间以共价键相结合成为冰 ②金属和非金属元素只能形成离子键
③离子键是阳离子、阴离子的相互吸引 ④两个非金属原子间不可能形成离子键
⑤所有物质中一定含有化学键
A. ①②⑤ B. 都不正确 C. ④ D. ②③④⑤
科目:高中化学 来源: 题型:
【题目】某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验。
Ⅰ.(1)将钠、钾、镁、铝各1 mol分别投入到足量的同浓度的盐酸中,试预测实验结果:_____与盐酸反应最剧烈,____与盐酸反应产生的气体最多。
(2)向Na2S溶液中通入氯气出现黄色浑浊,可证明非金属性:Cl____S(填“>”或“<”),反应的离子方程式为_______。
Ⅱ.利用如图装置可验证同主族元素非金属性的变化规律。

(3)仪器A的名称为___________,干燥管D的作用为___________________。
(4)若要证明非金属性:Cl>I,C中为淀粉—碘化钾混合溶液,B中装有KMnO4固体,则A中试剂为___________,观察到C中溶液____________(填现象),即可证明。从环境保护的观点考虑,此装置缺少尾气处理装置,可用_________溶液吸收尾气。
(5)若要证明非金属性:C>Si,则在A中加盐酸、B中加CaCO3、C中加Na2SiO3溶液。观察到C中溶液 ________(填现象),即可证明。但有的同学认为盐酸具有挥发性,HCl可进入C中干扰实验,应在两装置间添加装有 _________溶液的洗气瓶除去。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 蛋白质、纤维素、蔗糖、![]() 、淀粉都是高分子化合物
、淀粉都是高分子化合物
B. 蔗糖在人体内水解的产物只有葡萄糖
C. 使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用
D. 石油、煤、天然气、可燃冰都是化石燃料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用4 g单质锌与5mL 2 mol/L的稀硫酸作用制备氢气时,下列四种情况下生成氢气速率大小顺序为
①锌粒+硫酸 ②锌粉+硫酸 ③锌粉+硫酸+少量CuSO4粉末 ④锌粒+硫酸+少量3mol/L盐酸
A. ②>③>④>① B. ① >②>③> ④ C. ③>②>①>④ D. ②>①>③>④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁燃料电池具有比能量高、使用安全方便、原材料来源丰富、成本低、燃料易于贮运及污染小等特点。如图为镁——次氯酸盐燃料电池的工作原理图,下列有关说法不正确的是( )

A. 该燃料电池中镁为负极,发生氧化反应
B. 正极反应式为ClO―+H2O+2e―= Cl―+2OH―
C. 放电过程中OH―移向正极移动.
D. 电池总反应式为Mg+ClO―+H2O=Mg(OH)2↓+Cl―
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按如下方案可从样品粉末中提取具有抗肿瘤活性的天然产物A,下列每步实验所用装置、操作都正确的是

A. 步骤(1)  B. 步骤(2)
B. 步骤(2) C. 步骤(3)
C. 步骤(3) D. 步骤(4)
D. 步骤(4)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬水合物{[Cr(CH3COO)2]2·2H2O,相对分子质量为376}是一种深红色晶体,不溶于冷水,是常用的氧气吸收剂。实验室中以锌粒、三氯化铬溶液、醋酸钠溶液和盐酸为主要原料制备醋酸亚铬水合物,其装置如图所示,且仪器2中预先加入锌粒。已知二价铬不稳定,极易被氧气氧化,不与锌反应。制备过程中发生的相关反应如下:
Zn(s)+2HCl(aq)===ZnCl2(aq)+H2(g)
2CrCl3(aq)+Zn(s)===2CrCl2(aq)+ZnCl2(aq)
2Cr2+(aq)+4CH3COO-(aq)+2H2O(l)===[Cr(CH3COO)2]2·2H2O(s)
请回答下列问题:
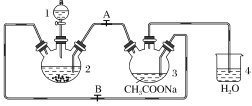
(1)仪器1的名称是________。
(2)往仪器2中加盐酸和三氯化铬溶液的顺序最好是________(选下面字母);目的是__________________________________________________________________。
A、盐酸和三氯化铬溶液同时加入
B.先加三氯化铬溶液一段时间后再加盐酸
C.先加盐酸一段时间后再加三氯化铬溶液
(3)为使生成的CrCl2溶液与CH3COONa溶液顺利混合,应关闭止水夹________(填“A”或“B”,下同),打开止水夹________。
(4)本实验中锌粒要过量,其原因除了让产生的H2将CrCl2溶液压入装置3与CH3COONa溶液反应外,另一个作用是____________________________。(用离子方程式表示)
(5)已知其它反应物足量,实验时取用的CrCl3溶液中含溶质9.51 g,取用的醋酸钠溶液为1.5 L 0.1 mol·L-1;实验后得干燥纯净的[Cr(CH3COO)2]2·2H2O 9.48 g,则该实验所得产品的产率为________(不考虑溶解的醋酸亚铬水合物)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个密闭容器中发生反应:2SO2(g)+O2(g)![]() 2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是
2SO3(g)。已知反应过程中的某一时间SO2、O2和SO3的浓度分别为:0.2mol/L、0.1mol/L和0.2mol/L。当反应达到平衡时可能存在的数据正确的是
A. c(O2)=0.2mol/LB. c(SO2)=0.25mol/L
C. c(SO2)+c(SO3)=0.3mol/LD. c(SO2)=c(SO3)=0.15mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com