
| 水浴 |
| 水浴 |
 、
、 、
、 ,二氧化碳和苯酚钠反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,
,二氧化碳和苯酚钠反应的离子方程式为C6H5O-+CO2+H2O→C6H5OH+HCO3-,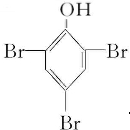 .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )
两种气态烃组成的混合气体完全燃烧后所得到CO2和H2O的物质的量随混合烃总物质的量的变化如图所示.下列有关混合气体的说法错误的是( )| A、该混合气体一定含有甲烷 |
| B、该混合气体中一定含有乙烯 |
| C、在110℃条件下,该混合气体与氧气混合,总混合气燃烧前后体积不变 |
| D、若混合气体由CH4和C2H4组成,则其体积比为2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
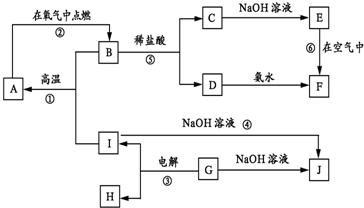
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 气体 | O2 | Cl2 | NH3 |
| 分液漏斗中试剂 | 浓氨水 | ||
| 圆底烧瓶中试剂 | KMnO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学键 | H-H | N-H | N≡N |
| 键能(kJ/mol) | 436 | 391 | 945 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1 mol?L-1的NH4Cl溶液中:c(Cl-)>c(NH4+)>c(H+)>c(OH-) |
| B、0.1 mol?L-1的CH3COONa溶液中:c(OH-)=c(H+)+c(CH3COOH) |
| C、0.1 mol?L-1的Na2S溶液中:c(Na+)=2[c(HS-)+c(S2-)+c(H2S)] |
| D、pH=2的盐酸与pH=12的氨水等体积混合后:c(Cl-)>c(NH4+)>c(OH-)>c(H+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com