
| A. | C2H4 C2H6 | B. | C2H4 C3H6 | C. | C2H4 C2H6O | D. | C2H6O C2H4O2 |
分析 物质的量相同的烃CxHy的耗氧量取决于x+$\frac{y}{4}$,物质的量相同的含烃氧衍生物CxHyOz耗氧量取决于x+$\frac{y}{4}$-$\frac{z}{2}$,据此判断物质的量相同各物质的耗氧量.
解答 解:物质的量相同的烃CxHy的耗氧量取决于x+$\frac{y}{4}$,物质的量相同的含烃氧衍生物CxHyOz耗氧量取决于x+$\frac{y}{4}$-$\frac{z}{2}$,
A.1molC2H4完全燃烧消耗3mol氧气,1molC2H6完全燃烧消耗3.5mol氧气,二者物质的量相同时充分燃烧耗氧量不同,故A不选;
B.1molC2H4完全燃烧消耗3mol氧气,1molC3H6完全燃烧消耗4.5mol氧气,二者物质的量相同时充分燃烧耗氧量不同,故B不选;
C.1mol完全燃烧消耗3mol氧气,1molC2H6O完全燃烧消耗3mol氧气,二者物质的量相同时充分燃烧耗氧量相同,故C选;
D.1molC2H6O完全燃烧消耗3mol氧气,1molC2H4O2完全燃烧消耗2mol氧气,二者物质的量相同时充分燃烧耗氧量不同,故D不选;
故选:C.
点评 本题考查有机物耗氧量规律,难度较小,掌握有机物耗氧量规律即可解答.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作 | 现象 | 结论 |
| A | 新制Fe(OH)2露置于空气中一段时间 | 白色固体迅速变为灰绿色,最终变为红褐色 | 说明Fe(OH)2易被氧化成Fe(OH)3 |
| B | 常温下将Fe片放入浓硝酸中 | 无明显变化 | Fe与浓硝酸不反应 |
| C | 将一小块Na放入医用酒精中 | 产生气泡 | Na只置换出醇羟基上的氢 |
| D | 向某无色溶液中滴加氯水和CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中有I- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 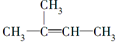 +Br2(CCl4)→ +Br2(CCl4)→ | |
| B. | CH2=CH-CH2-CH3+HCl$→_{△}^{催化剂}$ | |
| C. | CH3-CH=CH2+H2O$→_{加热、加压}^{催化剂}$ | |
| D. | CH4+Cl2$\stackrel{光照}{→}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
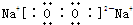 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分散质粒子大小都在1~100nm之间 | B. | 有丁达尔效应 | ||
| C. | 加热蒸干、灼烧后都有氧化铁生成 | D. | 呈红褐色 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验 编号 | 试管1中的试剂 | 试管2中试剂 | 测得有机层的厚度/cm |
| A | 3mL乙醇、2mL乙酸、1mL 18mol/L浓硫酸 | 饱和Na2CO3碳酸钠溶液 | 5.0 |
| B | 3mL乙醇、2mL乙酸 | 0.1 | |
| C | 3mL乙醇、2mL乙酸、6mL 3mol/L硫酸 | 1.2 | |
| D | 3mL乙醇、2mL乙酸、盐酸 | 1.2 |
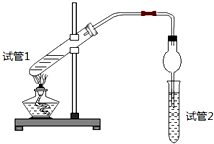 (1)写出实验A中试管1反应的化学方程式CH3COOH+C2H5OH
(1)写出实验A中试管1反应的化学方程式CH3COOH+C2H5OH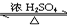 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤⑥之间的关系为同系物 | B. | ③⑥不是同分异构体 | ||
| C. | 可发生消去反应的有机物有4 | D. | 能被催化氧化为醛的有机物有4种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用托盘天平称量药品时,左盘放药品,右盘放砝码 | |
| B. | 向试管中滴加试剂时,将滴管下端紧靠试管内壁 | |
| C. | 用燃着的酒精灯去点燃另一酒精灯 | |
| D. | 使用试纸检验溶液的性质时,将试纸浸入溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 主族元素的最外层电子数都等于它的最高正化合价 | |
| B. | 同一主族的元素的原子最外层电子数相等 | |
| C. | 同周期的主族元素随核电荷数的递增原子半径逐渐减小 | |
| D. | 第N周期有N种主族元素是金属元素(N>1) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com