
【题目】如下图装置(夹持装置略,气密性已检验)某同学用含有铁锈(Fe2O3)的废铁屑来制取氯化铁晶体,下列推断不合理的是
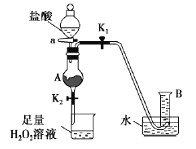
A.B中收集到的气体是氢气
B.烧杯中双氧水溶液作用是将Fe2+还原为Fe3+
C.A中的氧化铁与盐酸反应生成氯化铁
D.烧杯中溶液在氯化氢气氛下,蒸发浓缩、冷却结晶、过滤后得到氯化铁晶体
【答案】B
【解析】
A.铁和盐酸反应生成氯化亚铁和氢气,所以B中收集到的气体是氢气,A正确;
B.双氧水具有氧化性,可将Fe2+氧化为Fe3+,B错误;
C.氧化铁为碱性氧化物,可与盐酸反应生成氯化铁和水,C正确;
D.因铁离子易水解,制备氯化铁晶体,应在氯化氢气氛下,蒸发浓缩、冷却结晶、过滤后得到,D正确;
答案选B。
【点晴】
该题的难点和易错选项是D,在进行此类试题的分析与解答时,需要注意加热过程中溶质本身的变化。有关蒸干盐溶液所得物质的判断需要从以下几个角度(1)先考虑分解。如NaHCO3溶液、Ca(HCO3)2溶液蒸干灼烧得Na2CO3、CaCO3;KMnO4溶液蒸干灼烧得K2MnO4和MnO2。(2)考虑氧化还原反应。如加热蒸干Na2SO3溶液,所得固体为Na2SO4。(3)强酸弱碱盐水解生成挥发性酸的,蒸干后得到弱碱,水解生成不挥发性酸的,得到原物质。如AlCl3溶液蒸干得氢氧化铝,再灼烧得Al2O3;Al2(SO4)3溶液蒸干得本身。(4)弱酸强碱正盐溶液蒸干得到原物质,Na2CO3溶液蒸干得本身。(5)NH4Cl溶液、(NH4)2S溶液蒸干、灼烧,无残留物。(6)某些金属氯化物的结晶水合物,如MgCl2·6H2O和FeCl3·6H2O,在空气中加热时易发生水解,为得到其无水盐,通常将其结晶水合物在氯化氢气流中加热,以防止其水解。如MgCl2 · 6H2O![]() MgCl2 + 6H2O。
MgCl2 + 6H2O。


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
【题目】某含铬Cr2O72- 废水用硫酸亚铁铵[FeSO4·(NH4)2 SO4·6H2O]处理,反应中铁元素和铬元素完全转化为沉淀。该沉淀干燥后得到n molFeO·FeyCrxO3(Cr化合价+3价) 。不考虑处理过程中的实际损耗,下列叙述错误的是( )
A.消耗硫酸亚铁铵的物质的量为n(2-x)molB.处理废水中Cr2O72- 的物质的量为![]() mol
mol
C.反应中发生转移的电子为3nx molD.在FeO·FeyCrxO3中3x=y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯甲醛在医药、染料、香料等行业有着广泛的应用。实验室通过如图所示的流程由甲苯氧化制备苯甲醛。
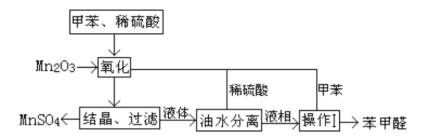
试回答下列问题:
(1)Mn2O3氧化甲苯的反应需要不断搅拌,搅拌的作用是___。
(2)甲苯经氧化后得到的混合物通过结晶、过滤进行分离,该过程中需将混合物冷却,其目的___。
(3)实验过程中,可循环使用的物质分别为___,___。
(4)实验中分离甲苯和苯甲醛采用的操作I是___________。
(5)实验中发现,反应时间不同苯甲醛的产率也不同(数据见下表),
反应时间/h | 1 | 2 | 3 | 4 | 5 |
苯甲醛产率/% | 76.0 | 87.5 | 83.6 | 72.5 | 64.8 |
请结合苯甲醛的结构,分析当反应时间过长时,苯甲醛产率下降的原因___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是一种丰富的资源,工业生产可以从海水中提取许多有用的物质,这些物质广泛应用于生活、生产、科技等方面。下图是从含碘CCl4溶液得到碘的实验过程:
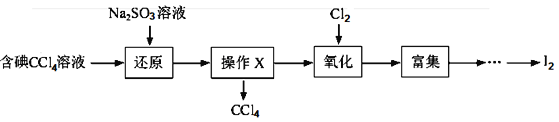
完成下列填空:
(1)向含碘溶液中加入稍过量的Na2SO3溶液,其离子方程式为_________;该操作将I2还原为I-的目的是__________。
(2)操作X的名称为_______,所用的主要仪器是_________。
(3)氧化时,在三颈瓶中将含I-的水溶液用盐酸调至pH约为2,缓慢通入Cl2,在400C左右反应(实验装置如图所示)。实验控制在较低温度下进行的原因是_________;锥形瓶里盛放的溶液为________。
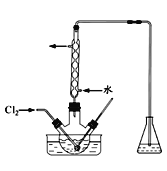
(4)已知:5SO32-+2IO3-+2H+ → I2+5SO42-+H2O某含碘溶液(pH约为8)中一定存在I2,可能存在I-、IO3—中的一种或两种。请补充完整检验含碘溶液中是否同时含有I-、IO3-的实验方案:_______。实验中可供选择的试剂:CCl4、稀盐酸、淀粉溶液
(5)浓海水提取镁的工艺流程如下图:
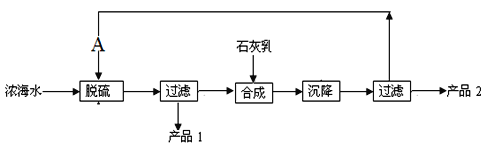
浓海水的主要成分如下:
离子 | Na+ | Mg2+ | Cl- | SO42- |
浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
该工艺过程中,脱硫阶段主要反应的离子方程式为________,产品2的化学式为__________。1L浓海水最多可得到产品2的质量为____g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某可逆反应mA(g)+nB(g)![]() qC(g),△H在密闭容器中进行。如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况。下列推断正确的是
qC(g),△H在密闭容器中进行。如图表示在不同时刻t、温度T和压强p下B物质在混合气体中的体积分数φ(B)的变化情况。下列推断正确的是

A. p1>p2,T1<T2,m+n>q,△H<0
B. p1<p2,T1>T2,m+n>q,△H>0
C. p1>p2,T1<T2,m+n<q,△H<0
D. p1<p2,T1>T2,m+n<q,△H>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
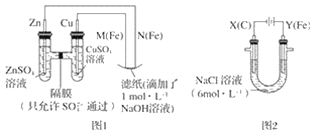
请回答:
Ⅰ.用图 1 所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代 Cu 作电极的是__(填字母序号)。
A 铝 B 石墨 C 银 D 铂
(2)N 极发生反应的电极反应式为__。
Ⅱ.用图 2 所示装置进行第二组实验。实验过程中,观察到与第一组实验不同的现象:两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。 查阅资料得知,高铁酸根离子(FeO42-)在溶液中呈紫红色。
(3)电解过程中,X 极区溶液的 pH__(填“增大”“减小”或“不变”)。
(4)电解过程中,Y 极发生的电极反应之一为 Fe﹣6e﹣+8OH﹣= FeO42-+4H2O 若在 X 极收集到672 mL 气体,在 Y 极收集到 168 mL 气体(均已折算为标准状况时气体体积),则 Y 电极(铁电极)质量减少____g。
(5)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为 2K2FeO4+3Z=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的反应的电极反应式为__。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中第VIIA族元素的单质及其化合物的用途广泛:
己知:H2CO3:Kal=4.3×l0-7 ,Ka2=5.6×l0-ll HC1O,Ka=2.98×l0-8
(1)室温下,0.l mol/L的次氯酸钠溶液和0.l mol/L的碳酸氢钠溶液,碱性较强的是___________;其原因是___________。
(2)己知新制氯水中存在三种分子和四种离子。在500mL l mol.L-l的碳酸钠溶液中,通入11.2L(标准状况)的Cl2,充分反应以后,溶液中离子浓度在前三位的大小顺序为__________;
(3)BrF3具有较强的氧化性,可以和许多还原剂反应。在一定条件下,BrF3和H2O反应生成O2和等物质的量的Br2和HBrO3,写出该反应的化学方程式_____________;
(4)向CuCl2溶液中滴加NaOH溶液,有蓝色沉淀生成,继续滴加一定量的NaHS溶液后,生成CuS黑色沉淀,用溶解平衡和电离平衡原理解释上述现象__________________;
(5)将1.12L(标准状况)CH3F在纯氧中完全燃烧,将产物通入足量的澄清石灰水中,溶液中有白色固体生成,白色沉淀是_____________、_________,再通入过量的CO2沉淀部分消失,继续滴加浓盐酸浊液变澄清,用离子方程式解释上述现象__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B. 乙烯与溴加成反应的产物为溴乙烷
C. 1 mol苯恰好与3 mol氢气完全加成,说明苯分子中有三个碳碳双键
D. 当n=7,主链上有5个碳原子的烷烃共有5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将17.6克Fe2O3和Cu的混合物溶解于足量的稀盐酸中,再加铁粉9.8克,待铁粉溶解后,溶液中无Fe3+,此过程共产生2.24升H2(标况),则下列判断正确的是
A.混合物中Cu全部被氧化为Cu2+以后,Cu2+又全部被还原
B.混合物中Cu全部被氧化为Cu2+以后,Cu2+又部分被还原
C.混合物中Cu部分被氧化为Cu2+以后,Cu2+又全部被还原
D.混合物中Cu部分被氧化为Cu2+以后,Cu2+又部分被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com