
【题目】某兴趣小组设计出如图所示装置来进行“铜与硝酸反应”实验,以探究化学实验的绿色化. 
(1)实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,其目的是 .
(2)在d中加适量NaOH溶液,c中放一小块铜片,由分液漏斗a向c中加入2mL浓硝酸,c中反应的化学方程式是 . 再由a向c中加2mL蒸馏水,c中的实验现象是 .
(3)如表是制取硝酸铜的三种方案,能体现绿色化学理念的最佳方案是 , 理由是、 .
方 案 | 反 应 物 |
甲 | Cu、浓HNO3 |
乙 | Cu、稀HNO3 |
丙 | Cu、O2、稀HNO3 |
(4)该小组还用上述装置进行实验证明氧化性KMnO4>Cl2>Br2 . 操作步骤为:实验现象为 .
【答案】
(1)检查装置气密性
(2)Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;反应变缓,红棕色气体逐渐变为无色
(3)丙;制取等量的硝酸铜时,丙方案耗酸量最少;无污染物(NOX)产生
(4)a中加入浓盐酸,c中加入高锰酸钾,d中加入溴化钾溶液 、 打开b由a向c中加入浓盐酸; c中有黄绿色气体产生,d中溶液由无色变为橙黄色 ;但此实验的不足之处是 无尾气处理装置,会污染环境
【解析】解:(1)实验前要检查装置气密性,实验前,关闭活塞b,试管d中加水至浸没长导管口,塞紧试管c和d的胶塞,加热c,这是检查装置气密性的常见方法,
所以答案是:检查装置气密性;(2)铜与浓硝酸反应得到硝酸铜、二氧化氮和水,反应的化学方程式为:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;由a向c中加2mL蒸馏水,硝酸进行的稀释,反应变缓,同时二氧化氮能与水反应生成硝酸和一氧化氮,故c中气体颜色红棕色气体逐渐变为无色,
所以答案是:Cu+4HNO3=Cu(NO3)2+2NO2↑+2H2O;反应变缓,红棕色气体逐渐变为无色;(3)甲:铜与浓硝酸制取硝酸铜时的方程式是:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,生成的NO2会造成大气污染,硝酸的利用率为50%;
乙:铜与稀硝酸制取硝酸铜时的方程式是:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O,生成的NO也会造成大气污染,硝酸的利用率为75%;
丙:此过程用方程式可表示为:2Cu+O2 ![]() 2CuO,CuO+2HNO3=Cu(NO3)2+H2O,从过程可以看出该过程不会产生有毒气体,环保且没有多消耗原料,故能体现绿色化学理念的最佳方案是丙,
2CuO,CuO+2HNO3=Cu(NO3)2+H2O,从过程可以看出该过程不会产生有毒气体,环保且没有多消耗原料,故能体现绿色化学理念的最佳方案是丙,
所以答案是:丙;制取等量的硝酸铜时,丙方案耗酸量最少;无污染物(NOX)产生;(4)根据氧化还原反应中氧化剂的氧化性大于氧化产物的氧化性,利用KMnO4与浓盐酸反应:2KMnO4+16HCl=2KCl+2MnCl2+5Cl2↑+8H2O,
再利用产生的氯气与KBr溶液反应得到溴:Cl2+2KBr=2KCl+Br2,操作步骤为a中加入浓盐酸,c中加入高锰酸钾,d中加入溴化钾溶液,打开b由a向c中加入浓盐酸,现象为c中有黄绿色气体产生,d中溶液变为橙色,同时要注意尾气吸收,防止污染空气,
所以答案是:a中加入浓盐酸,c中加入高锰酸钾,d中加入溴化钾溶液;打开b由a向c中加入浓盐酸;c中有黄绿色气体产生,d中溶液由无色变为橙黄色;无尾气处理装置,会污染环境.


科目:高中化学 来源: 题型:
【题目】肼可作为火箭发动机的燃料,与N2O4反应生成N2和水蒸气.已知:
①N2(g)+2O2(g)=N2O4(l)△H1=﹣19.5kJmol﹣1
②N2H4(l)+O2(g)=N2(g)+2H2O(g)△H2=﹣534.2kJmol﹣1
(1)写出肼和N2O4反应反应生成N2和水蒸气的热化学方程式;
(2)火箭残骸中常现红棕色气体,当温度升高时,气体颜色变深,原因是存在如下反应:N2O4(g)2NO2(g)△H>0,一定温度下,将1mol N2O4充入一恒压密闭容器中发生上述反应,下列示意图正确且能说明反应达到平衡状态的是 . 
(3)肼﹣空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.肼﹣空气燃料电池放电时负极的电极反应式是 .
(4)传统制备肼的方法,是以NaClO氧化NH3 , 制得肼的稀溶液.该反应的离子方程式是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学科研小组在其他条件不变时,改变某一条件对反应[可用aA(g)+bB(g)cC(g)表示]的化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率).根据图象,下列判断正确的是( )
A.
如图反应:若p1>p2 , 则此反应只能在高温下自发进行
B.
如图反应:此反应的△H<0,且T1<T2
C.
如图反应:表示t1时刻一定是使用催化剂对反应速率的影响
D.
如图反应:表示t1时刻增大B的浓度对反应速率的影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据相应的图象(图象编号与答案一一对应),判断下列相关说法正确的是( )
A.
密闭容器中反应达到平衡,T0时改变某一条件有如图变化所示,则改变的条件一定是加入催化剂
B.
反应达到平衡时,外界条件对平衡影响关系如图所示,则正反应为放热反应,且a>b
C.
物质的百分含量和温度关系如图所示,则该反应的正反应为吸热反应
D.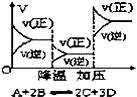
反应速率和反应条件变化关系如图所示,则该反应的正反应为放热反应,A,B,C是气体、D为固体或液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用CO合成甲醇(CH3OH)的化学方程式为CO(g)+2H2(g)CH3OH(g)△H<0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( ) 
A.温度:T1>T2>T3
B.平衡常数:K(a)>K(c) K(b)=K(d)
C.正反应速率:v(a)>v(c) v(b)>v(d)
D.平均摩尔质量:M(a)<M(c) M(b)>M(d)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示不同温度下水溶液中c(H+)与c(OH﹣)的关系,下列判断正确的是( ) 
A.两条曲线上任意点均有c(H+)×c (OH﹣)=Kw
B.T<25
C.b点和c点pH均为6,溶液呈酸性
D.只采用升温的方式,可由a点变成d点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,在一定体积pH=12的Ba(OH)2溶液中逐滴加入一定物质的量浓度的NaHSO4溶液,当溶液中的Ba2+恰好完全沉淀时,溶液pH=11.若体积可以加和,则V(Ba(OH)2):V( NaHSO4)为( )
A.1:1
B.1:2
C.1:3
D.1:4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如下(部分反应条件及产物略去). A ![]() B
B ![]() C
C
(1)若A是一种黄色单质固体,则B→C的化学方程式为 .
(2)若A是一种活泼金属,C是淡黄色固体,试用化学方程式表示C与二氧化碳气体的反应 . 将C长期露置于空气中,最后将变成物质D,D的化学式为 . 现有D和NaHCO3的固体混合物10.0g,加热至质量不再改变,剩余固体质量为9.38g,D的质量分数为 .
(3)若C是红棕色气体,如图是实验室制取A气体的装置,请结合所学知识,回答下列问题: 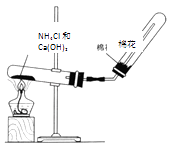
①试写出由A到B的化学方程式 .
②验证A是否已经收集满的方法是(任写一种).
③写出工业上制取A的化学方程式 .
④C与水反应可得到酸X,要使1molC恰好完全转化为X,需通入氧气的物质的量为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用pH试纸测定某无色溶液的pH时,规范的操作是( )
A. 将pH试纸放入溶液中观察其颜色变化,跟标准比色卡比较
B. 将溶液倒在pH试纸上,跟标准比色卡比较
C. 用干燥的洁净玻璃棒蘸取溶液,滴在pH试纸上跟标准比色卡比较
D. 试管内放少量溶液,煮沸,把pH试纸放在管口,观察颜色,跟标准比色卡比较
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com