
| A、①③ | B、②④ | C、①④ | D、②③ |


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:高中化学 来源: 题型:
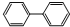 ,下列有关联苯的说法中正确的是( )
,下列有关联苯的说法中正确的是( )| A、分子中含有6个碳碳双键 |
| B、联苯的一硝基取代产物的3种 |
| C、它容易发生加成反应、取代反应,容易被强氧化剂氧化 |
D、它和蒽(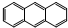 )同属于芳香烃,两者互为同系物 )同属于芳香烃,两者互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:A<B<C |
| B、C的最简单氢化物的稳定性大于A的最简单氢化物的稳定性 |
| C、高温下,A单质能置换出C单质 |
| D、三种元素的最高价氧化物对应的水化物均可由化合反应得到 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯化钠溶液在电流作用下电离成Na+与Cl? |
| B、溶于水后能电离出H+的化合物都是酸 |
| C、氯化氢溶于水后能导电,但液态氯化氢不能导电 |
| D、导电性强的溶液中自由移动离子数目一定比导电性弱的溶液中自由移动离子数目多 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、-(6-3n) |
| B、-(8-n) |
| C、-(12-3n) |
| D、-(14-5n) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
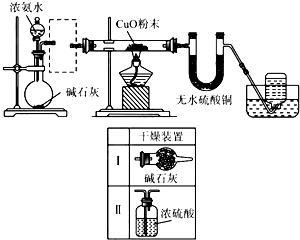 实验室进行某项实验并检验反应产物的装置如图.
实验室进行某项实验并检验反应产物的装置如图.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com