
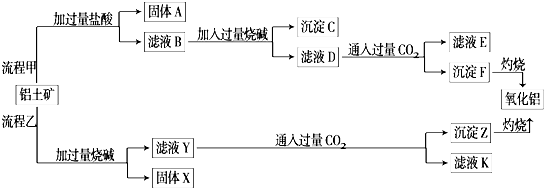
分析 铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中加入稀盐酸,Al2O3、Fe2O3、MgO分别和稀盐酸反应生成AlCl3、FeCl3、MgCl2,SiO2不溶于稀盐酸,然后过滤得到的A为SiO2,向滤液B中加入过量烧碱,AlCl3、FeCl3、MgCl2分别和NaOH反应生成可溶性的NaAlO2和沉淀Fe(OH)3、Mg(OH)2,然后再过滤,向滤液中通入过量二氧化碳,生成Al(OH)3沉淀同时生成可溶性NaHCO3,再过滤,滤液E中溶质成分是NaHCO3,沉淀F是Al(OH)3,将沉淀F灼烧得到氧化铝;
铝土矿中加入过量NaOH溶液,Al2O3、SiO2溶于氢氧化钠分别得到可溶性的NaAlO2、Na2SiO3,Fe2O3、MgO不溶于NaOH溶液,然后过滤得到固体X为Fe2O3、MgO,滤液Y中含有NaOH、NaAlO2、Na2SiO3,向滤液中通入过量二氧化碳,得到沉淀Z为Al(OH)3、H2SiO3,滤液中K为NaHCO3,灼烧氢氧化铝和硅酸分别得到氧化铝和二氧化硅;
(1)流程甲中D溶液中通入过量的CO2生成碳酸氢钠和氢氧化铝;
(2)二氧化硅和NaOH反应生成硅酸钠和水;
(3)铁离子和KSCN溶液反应生成络合物而使溶液呈血红色;
(4)①锌和氢氧化钠溶液反应生成偏锌酸钠和氢气;
②两种溶液,用相互滴加的实验方法即可鉴别说明其反应现象不同;
③氢氧化锌能溶于过量氨水中.
解答 解:铝土矿(主要成分是Al2O3,含SiO2、Fe2O3、MgO等杂质)中加入稀盐酸,Al2O3、Fe2O3、MgO分别和稀盐酸反应生成AlCl3、FeCl3、MgCl2,SiO2不溶于稀盐酸,然后过滤得到的A为SiO2,向滤液B中加入过量烧碱,AlCl3、FeCl3、MgCl2分别和NaOH反应生成可溶性的NaAlO2和沉淀Fe(OH)3、Mg(OH)2,然后再过滤,向滤液中通入过量二氧化碳,生成Al(OH)3沉淀同时生成可溶性NaHCO3,再过滤,滤液E中溶质成分是NaHCO3,沉淀F是Al(OH)3,将沉淀F灼烧得到氧化铝;
铝土矿中加入过量NaOH溶液,Al2O3、SiO2溶于氢氧化钠分别得到可溶性的NaAlO2、Na2SiO3,Fe2O3、MgO不溶于NaOH溶液,然后过滤得到固体X为Fe2O3、MgO,滤液Y中含有NaOH、NaAlO2、Na2SiO3,向滤液中通入过量二氧化碳,得到沉淀Z为Al(OH)3、H2SiO3,滤液中K为NaHCO3,灼烧氢氧化铝和硅酸分别得到氧化铝和二氧化硅;
(1)流程甲中D溶液中通入过量的CO2生成碳酸氢钠和氢氧化铝,离子方程式为AlO2-+2H2O+CO2═Al(OH)3↓+HCO3ˉ,故答案为:AlO2-+2H2O+CO2═Al(OH)3↓+HCO3ˉ;
(2)二氧化硅和NaOH反应生成硅酸钠和水,离子反应方程式为SiO2+2OH-═SiO32-+H2O,故答案为:SiO2+2OH-═SiO32-+H2O;
(3)铁离子和KSCN溶液反应生成络合物而使溶液呈血红色,所以可以用KSCN溶液检验铁离子,故答案为:硫氰化钾;
(4)①锌和氢氧化钠溶液反应生成偏锌酸钠和氢气,反应方程式为Zn+2NaOH═Na2ZnO2+H2↑,故答案为:Zn+2NaOH═Na2ZnO2+H2↑;
②两种溶液,用相互滴加的实验方法即可鉴别说明其反应现象不同,
A.向硫酸铝中加入NaOH溶液,先生成沉淀后沉淀溶解,向氢氧化钠溶液中加入硫酸铝溶液,先没有沉淀生成后产生沉淀,所以现象不同,可以鉴别,故A正确;
B.硫酸铝、氨水相互滴加都生成白色沉淀,所以无法鉴别,故B错误;
C.向硫酸锌溶液中加入NaOH溶液先生成白色沉淀后沉淀溶解,向氢氧化钠中加入硫酸锌溶液,先没有沉淀生成后产生沉淀,所以现象不同,可以鉴别,故C正确;
D.向硫酸锌溶液中加入氨水溶液先生成白色沉淀后沉淀溶解,向氨水中加入硫酸锌溶液,先没有沉淀生成后产生沉淀,所以现象不同,可以鉴别,故D正确;
故选ACD;
③可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成[Zn(NH3)4]2+,氨水的用量不易控制,所以不能用硫酸锌和氨水制取氢氧化锌,故答案为:可溶性锌盐与氨水反应产生的Zn(OH)2可溶于过量氨水中,生成[Zn(NH3)4]2+,氨水的用量不易控制.
点评 本题考查物质的分离和提纯,为高频考点,侧重考查学生分析推断、知识迁移能力,明确元素化合物性质是解本题关键,知道流程图中发生的反应及操作方法,注意氢氧化锌能溶于氨水,题目难度不大.


科目:高中化学 来源: 题型:解答题
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 叙述I | 叙述II |
| A | 苯甲酸的溶解度随温度升高而增大 | 用蒸发浓缩、冷却结晶、过滤,除去苯甲酸中混有的泥沙 |
| B | NH4Cl受热容易分解 | 加热NH4Cl制备NH3 |
| C | SO2具有漂白性 | SO2能使酸性KMnO4溶液褪色 |
| D | 某温度下,碳酸的K1=4.4×10-7,次氯酸的K=2.98×10-8 | 用CO2和NaClO溶液制备HClO |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKap | 37.4 | 19.3 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 物质的量相等的185Hf与180Hf质量相同 | |
| B. | 核外电子数分别为108、113 | |
| C. | 1 mol 180Hf比1 mol 185Hf的中子数少5NA | |
| D. | 180Hf、185Hf在周期表中的位置不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碱性:KOH>NaOH | B. | 相对原子质量:Ar>K | ||
| C. | 酸性HClO4>H2SO4 | D. | 元素的金属性:Mg>Al |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com