
【题目】设计出燃料电池使汽油氧化直接产生电流是本世纪最具有挑战性的课题之一。最近有人制造了一种燃料电池,一个极通入空气,另一个极通入汽油蒸气,电池的电解质是掺杂了Y2O3的ZrO2晶体,它在高温下能传导O2-,回答如下问题:
⑴以丁烷为汽油代表,这个电池放电时发生的化学反应的方程式是:_______;
⑵这个电池负极发生的反应是:C4H10+13O2--26e-=4CO2+5H2O,正极发生的反应是:____;固体电解质里O2-的移动方向是:_____;向外电路释放电子的电极是:___;
⑶人们追求燃料电池氧化汽油而不在内燃机里燃烧汽油产生动力的主要原因是:_______;
⑷汽油燃料电池最大的障碍是氧化反应不完全产生_____堵塞电极的气体通道,有人估计,完全避免这种副反应至少还需10年,这正是新一代化学家的历史使命。
⑸碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2,溶于水达到平衡时,溶液的溶液的pH=5.6, c(H2CO3)=1.5×10-5mol·L-1。若忽略水的电离及H2CO3的第二级电离,则H2CO3 H++HCO3-的平衡常数K1=____(已知:10-5.60=2.5×10-6)。
【答案】2C4H10+13O2=8CO2+10H2O O2+4e-=2O2- 向负极移动 负极 燃料电池具有较高的能量利用率 碳粒 4.2×10-7
【解析】
(1)燃料电池的总反应和燃料燃烧的化学方程式一致,则电池总反应为2C4H10+13O2=8CO2+10H2O,故答案为:2C4H10+13O2=8CO2+10H2O;
(2)丁烷燃料电池放电时,氧气在正极得到电子发生还原反应生成O2-,电极反应式为O2+4e-=2O2-,电解质里的阳离子移向正极,阴离子移向负极,所以电解质里O2-移向负极,负极上甲烷失去电子发生氧化反应,向外电路释放电子,故答案为:O2+4e-=2O2-;向负极移动;负极;
(3)原电池具有能量利用率高的特点,而燃烧时化学能转变为热能和光能,故答案为:燃料电池具有较高的能量利用率;
(4)烷不完全氧化会生成碳粒,从而堵塞电极的气体通道,故答案为:碳粒;
(5)由题意可知,溶液中c(H+)=c(HCO3-)=10-5.60=2.5×10-6mol/L,c(H2CO3)=1.5×10-5mol L,则H2CO3 ![]() H++HCO3-的平衡常数K1=
H++HCO3-的平衡常数K1=![]() =
=![]() =4.2×10-7,故答案为:=4.2×10-7。
=4.2×10-7,故答案为:=4.2×10-7。


科目:高中化学 来源: 题型:
【题目】甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如下图所示(部分产物已略去),下列各组物质中不能按图示关系转化的是
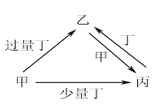
选项 | 甲 | 乙 | 丙 | 丁 |
A | NaOH | NaHSO3 | Na2SO3 | SO2 |
B | Fe | Fe(NO3)3 | Fe(NO3)2 | HNO3 |
C | C | CO2 | CO | O2 |
D | Al | NaAlO2 | Al(OH)3 | NaOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.利用一束强光照射明矾溶液,产生光亮的“通路”,说明明矾一定发生了水解
B.与Al反应放出![]() 的溶液中
的溶液中![]() 、
、![]() 、
、![]() 、
、![]() 有可能大量共存
有可能大量共存
C.![]() 溶液中通入过量
溶液中通入过量![]() 的离子方程式:
的离子方程式:![]()
D.等体积、等物质的量浓度的NaX溶液和弱酸HX混合后的溶液中![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(2017·天津卷)常压下羰基化法精炼镍的原理为:Ni(s)+4CO(g)![]() Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
Ni(CO)4(g)。230℃时,该反应的平衡常数K=2×105。已知:Ni(CO)4的沸点为42.2℃,固体杂质不参与反应。
第一阶段:将粗镍与CO反应转化成气态Ni(CO)4;
第二阶段:将第一阶段反应后的气体分离出来,加热至230℃制得高纯镍。
下列判断正确的是
A. 增加c(CO),平衡向正向移动,反应的平衡常数增大
B. 第二阶段,Ni(CO)4分解率较低
C. 第一阶段,在30℃和50℃两者之间选择反应温度,选50℃
D. 该反应达到平衡时,v生成[Ni(CO)4]=4v生成(CO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】四种短周期元素X、Y、Z、W的最外层电子数之和为16,其中X、Y、Z的电子层数相同,W原子的核外电子层数与其他三种不同,X元素的焰色反应呈黄色,Y元素能形成多种单质,其中一种单质在空气中易自燃,Z元素的最外层电子数是K层的2倍。下列推断正确的是( )
A.原子半径:X<Y
B.简单离子半径:W>X>Y
C.Z和W形成的化合物和某些酸、强碱均能发生反应
D.X、Y、W和氢元素形成的化合物的水溶液一定呈碱性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】顺铂[Pt(NH3)2Cl2]是1969年发现的第一种具有抗癌活性的金属配合物;碳铂是1,1-环丁二羧酸二氨合铂(Ⅱ)的简称,属于第二代铂族抗癌药物,结构简式如图所示,其毒副作用低于顺铂。下列说法正确的是( )
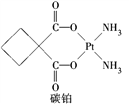
A. 碳铂中所有碳原子在同一个平面中
B. 顺铂分子中氮原子的杂化方式是sp2
C. 碳铂分子中sp3杂化的碳原子与sp2杂化的碳原子之比为2∶1
D. 1 mol 1,1-环丁二羧酸含有σ键的数目为12NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z、W是原子序数依次增大的前四周期元素,X、Z的周期序数=族序数,由这四种元素组成的单质或化合物存在如图所示的转化关系,其中甲、戊是两常见的金属单质,丁是非金属单质,其余为氧化物且丙为具有磁性的黑色晶体。下列说法正确的是

A. W的原子序数是Z的两倍,金属性强于Z
B. W元素在周期表中的位置是第四周期VIII族
C. 丙属于两性氧化物
D. 等物质的量的甲和戊完全溶于稀硝酸,消耗的HNO3的量一定相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列几种情况,对中和滴定结果无影响的是
A.滴定管用水冲洗后即注入标准液B.锥形瓶里有少量水
C.滴定前标准液在“0”刻度以上D.滴定管尖端未充满液体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.食醋常用于食品调味,其主要成分为醋酸。请回答:
(1)写出醋酸的电离方程式________________
(2)0.1mol/L醋酸溶液中加入少量盐酸,电离平衡向___反应方向移动(填“正”或“逆”)。
(3)在0.1mol/L醋酸溶液中加入少量醋酸钠晶体,晶体溶解后,醋酸溶液的pH____(选填“增大”“减小”或“不变”)。
(4)0.1mol/L醋酸溶液的pH____(选填“>”“=”或“<”)0.1mol/L盐酸溶液的pH。
(5)在0.1mol/L醋酸溶液中加入等体积等浓度的氢氧化钠溶液,反应后溶液显____性。
II.某同学想用实验确定CH3COOH是弱电解质。其方案是:
①称取一定质量的CH3COOH配制0.1molL-1的溶液100mL;
②用pH试纸测出该溶液的pH,即可证明HCOOH是弱电解质。
(1)方案的第①步中,要用到的玻璃定量仪器是______。
(2)该方案中,说明CH3COOH是弱电解质的理由是测得溶液的pH______1(选填>、<、=)。
(3)结合你所学的知识,试再提出一个简单易操作的可行方案证明CH3COOH是弱电解质(药品可任取)。_______________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com