
【题目】下列行为符合安全要求的是( )
A. 不慎洒出的酒精在实验台上着火时, 立即用水扑灭
B. 金属钠着火时, 立即用湿毛巾扑灭
C. 大量氯气泄漏时, 迅速离开现场并尽量向高处撤离
D. 稀释浓硫酸时, 将水倒入浓硫酸中并不断搅拌
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】检验HCl气体中是否混有少量Cl2可采用的方法是
A. 凭气味和颜色 B. 通入AgNO3溶液
C. 干燥的蓝色石蕊试纸,观察其颜色变化 D. 紫色石蕊试液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】煤化工中常需研究不同温度下平衡常数、投料比等问题.已知:CO (g)+H2O (g)H2 (g)+CO2 (g)平衡常数K随温度的变化如下表:
温度/℃ | 400 | 500 | 800 |
平衡常数K | 9.94 | 9 | 1 |
回答下列问题
(1)该反应的平衡常数表达式K= , △H=0(填“<”、“>”、“=”)
(2)已在一定温度下,C(s)+CO2 (g)2CO (g)平衡常数K1;
C (s)+H2O(g)CO(g)+H2 (g)平衡常数K2则K、K1、K2 , 之间的关系是;
(3)800℃时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时间后反应达到平衡,此时CO的转化率为:若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40molCO2 , 此时v正v逆 (填“>”、“=”或“<”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硝酸与合成氨工业密切相关,氨氧化法是工业生产中制取硝酸的主要途径.完成下列计算:
(1)合成氨时,假设100L的氮气与氢气(体积比为1:3)的混合气体通过氨合成塔充分反应后,体积变为90L,则氮气的转化率为 . (写出计算过程,计算结果请用百分数表示)
(2)标准状况下,将500L氨气溶于1L水中形成氨水,则此氨水质量分数为 . (写出计算过程,计算结果请用百分数表示,并保留1位小数)
(3)氨氧化法是将氨和空气的混合气通过灼热的铂铑合金网,在合金网的催化下,氨被氧化成一氧化氮(NO).此时温度很高,水以水蒸气的形式存在,NO也不与O2反应.若氨气与氧气物质的量之比为1:1.7时,氨的转化率可达95%,计算反应后NO的体积分数 . (设氧气在空气中的体积分数为20%,写出计算过程,计算结果请用百分数表示并保留1位小数)
(4)一氧化氮继续氧化为二氧化氮,二氧化氮溶于水可得硝酸.为测定某18K金样品的组成,将2.832g样品粉碎后投入足量的浓硝酸中,充分溶解后,收集到NO2和N2O4的混合气体224mL(折算至标准状况,下同),将该混合气体与84mL O2混合后缓缓通入水中,恰好被完全吸收.( 已知金不溶于浓硝酸) 填写该18K金的成分表(写出计算过程,计算结果请用百分数表示并保留1位小数,若不含该金属则填0).
18K金成分 | Au | Ag | Cu |
含量(质量分数) | 75% |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁炭混合物(铁屑和活性炭的混合物)、纳米铁粉均可用于处理水中污染物.
(1)铁炭混合物在水溶液中可形成许多微电池.将含有Cr2O72﹣的酸性废水通过铁炭混合物,在微电池正极上Cr2O72﹣转化为Cr3+ , 其电极反应式为 .
(2)在相同条件下,测量总质量相同、铁的质量分数不同的铁炭混合物对水中Cu2+和Pb2+的去除率,结果如图1所示. 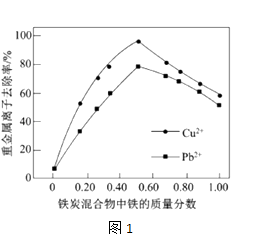
①当铁炭混合物中铁的质量分数为0时,也能去除水中少量的Cu2+和Pb2+ , 其原因是 .
②当铁炭混合物中铁的质量分数大于50%时,随着铁的质量分数的增加,Cu2+和Pb2+的去除率不升反降,其主要原因是 .
(3)纳米铁粉可用于处理地下水中的污染物. ①一定条件下,向FeSO4溶液中滴加碱性NaBH4溶液,溶液中BH4﹣(B元素的化合价为+3)与Fe2+反应生成纳米铁粉、H2和B(OH)4﹣ , 其离子方程式为 .
②纳米铁粉与水中NO3﹣反应的离子方程式为4Fe+NO3﹣+10H+=4Fe2++NH4++3H2O
研究发现,若pH偏低将会导致NO3﹣的去除率下降,其原因是 .
③相同条件下,纳米铁粉去除不同水样中NO3﹣的速率有较大差异(见图2),产生该差异的可能原因是 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理分析解答以下问题:
(1)弱酸在水溶液中存在电离平衡,部分0.1molL﹣1弱酸的电离平衡常数如下表:
弱酸 | 电离平衡常数(25℃) |
HClO | K=2.98×10﹣8 |
H2CO3 | K1=4.3×10﹣7 |
H2SO3 | K1=1.54×10﹣2 |
①当弱酸的浓度一定时,降低温度,K值(填“变大”“变小”或“不变”).
②下列离子方程式和有关说法错误的是 .
a.少量的CO2通入次氯酸钠溶液中:2ClO﹣+H2O+CO2═2HClO+CO32﹣
b.少量的SO2通入碳酸钠溶液中:SO2+H2O+2CO32﹣═2HCO3﹣+SO32﹣
c.相同温度时,等物质的量浓度的三种弱酸与足量NaOH溶液完全中和消耗NaOH的体积为V(H2CO3)>V(H2SO3)>V(HClO)
d.相同温度时,等pH三种盐溶液的物质的量浓度关系:c(Na2CO3)<c(NaClO)<c(Na2SO3)
③亚硒酸(H2SeO3)也是一种二元弱酸,有较强的氧化性.往亚硒酸溶液中不断通入SO2会产生红褐色单质,写出该反应的化学方程式: .
(2)工业废水中常含有一定量的Cr2O72﹣和CrO42﹣ , 它们对人类及生态系统会产生很大损害,必须进行处理后方可排放. ①在废水中存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O.若改变条件使上述平衡向逆反应方向移动,则下列说法正确的是 .
a.平衡常数K值可以不改变
b.达到新平衡CrO42﹣的消耗速率等于Cr2O72﹣的消耗速率
c.达到新平衡后,溶液pH一定增大
d.再达平衡前逆反应速率一定大于正反应速率
②Cr2O72﹣和CrO42﹣最终生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)Cr3+(aq)+3OH﹣(aq),常温下Cr(OH)3的Ksp=10﹣32 , 当c(Cr3+)降至10﹣3 molL﹣1 , 溶液的pH调至4时,(填“有”或“没有”)沉淀产生.
(3)已知:①2CH3OH(g)CH3OCH3(g)+H2O(g) ②CO(g)+2H2(g)CH3OH(g)
③CO(g)+H2O(g) CO2(g)+H2(g)
某温度下三个反应的平衡常数的值依次为K1、K2、K3 , 则该温度下反应3CO(g)+3H2(g)CH3OCH3(g)+CO2(g)的化学平衡常数K=(用含K1、K2、K3的代数式表示).向某固定体积的密闭容器中加入3mol CO和3mol H2 , 充分反应后恢复至原温度,测定容器的压强为反应前的 ![]() ,则CO的转化率为 .
,则CO的转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B两种有机物的分子式相同,都可用CaHbOcNd表示,且a+c=b,a-c=d。已知A是天然蛋白质水解的最终产物;B是一种含有醛基的硝酸酯。试回答:
(1)A和B的分子式是________________。
(2)光谱测定显示,A的分子结构中不存在甲基,则A的结构简式为_______________________。
(3)光谱测定显示,B的烃基中没有支链,则B的结构简式为_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X-的核外电子排布为2、8、8,则X元素在周期表中的位置是( )
A.第三周期第0族B.第四周期第ⅠA族
C.第三周期第ⅠA族D.第三周期第ⅦA族
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com