
【题目】下图是三种有机物的结构,请回答下列问题。
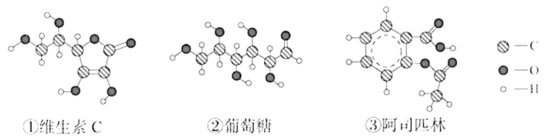
(1)能发生水解的是______________(填序号)。
(2)能发生加成反应的是____________(填序号)。
(3)1mol阿司匹林与足量的NaOH反应,消耗NaOH的物质的量是____________mol。
(4)下列说法正确的是____________(填字母序号 )。
a.阿司匹林属于芳香烃
b.维生素C分子式是C6H8O6
c.维生素C和葡萄糖均有还原性
d.葡萄糖是人体内重要的供能物质
【答案】①③ ①②③ 3 bcd
【解析】
维生素C的结构简式为 ,分子中含有碳碳双键、羟基、酯基;葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,分子中含有醛基和羟基;阿司匹林结构简式为
,分子中含有碳碳双键、羟基、酯基;葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,分子中含有醛基和羟基;阿司匹林结构简式为![]() ,分子中含有羧基和酯基,据此分析。
,分子中含有羧基和酯基,据此分析。
维生素C的结构简式为 ,分子中含有碳碳双键、羟基、酯基;葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,分子中含有醛基和羟基;阿司匹林结构简式为
,分子中含有碳碳双键、羟基、酯基;葡萄糖的结构简式为CH2OH—CHOH—CHOH—CHOH—CHOH—CHO,分子中含有醛基和羟基;阿司匹林结构简式为![]() ,分子中含有羧基和酯基。
,分子中含有羧基和酯基。
(1)维生素C和阿司匹林中均含有酯基,能发生水解反应,答案为①③;
(2)维生素C中含有碳碳双键、葡萄糖中含有醛基、阿司匹林中含有苯环,均能与氢气发生加成反应,答案为①②③;
(3)阿司匹林结构简式为![]() ,分子中含有1个羧基和1个酯基(且水解产物含有酚羟基),1mol阿司匹林与足量的NaOH反应,消耗NaOH的物质的量是3mol;
,分子中含有1个羧基和1个酯基(且水解产物含有酚羟基),1mol阿司匹林与足量的NaOH反应,消耗NaOH的物质的量是3mol;
(4)a.阿司匹林中含有O元素,不属于芳香烃,属于芳香族化合物,选项a错误;
b. 维生素C的结构简式为 ,分子式是C6H8O6,选项b正确;
,分子式是C6H8O6,选项b正确;
c.维生素C含有碳碳双键及羟基、葡萄糖中含有醛基和羟基,均有还原性,选项c正确;
d.葡萄糖是人体内重要的供能物质,选项d正确;
答案选bcd。


科目:高中化学 来源: 题型:
【题目】有机物 X 分子式为C3H6O,有多种同分异构体。其中之一丙醛(液态)的燃烧热为1815kJ/mol。下列说法不正确的是
A.X 的同分异构体中,含单官能团的共 5 种
B.1mol X 最多能和 1mol H2 加成
C.表示丙醛燃烧热的热化学方程式为:C3H6O(l)+4O2(g) = 3CO2 (g)+3H2O(l) △H=+1815kJ/mol
D.X 的同分异构体其中之一 CH2=CHCH2OH 可以发生取代反应、加成反应、加聚反应、氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】As2O3(砒霜)是两性氧化物(分子结构如图所示),溶于盐酸生成 AsCl3,AsCl3用 LiAlH4还原生成 AlH3。下列说法正确的是( )

A.As2O3 分子中 As 原子的杂化方式为 sp
B.LiAlH4为共价化合物
C.AsCl3空间构型为平面正三角形
D.AlH3分子键角大于 109.5°
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究有机物A的组成与结构,某同学进行如下实验。
i.将9.0gA 在足量氧气中充分燃烧,并使其产物依次缓缓通过足量的浓硫酸和碱石灰,发现两者分别增重5.4g和13.2g。
ii.通过质谱法测得其相对分子质量为90。
ili.通过红外光谱法测得A中含有—OH和—COOH。
请回答下列问题。
(1)9.0gA完全燃烧生成水的物质的量是____________mol。
(2)A的实验式是____________。
(3)A的分子式是____________。
(4)在一定条件下,若两个A分子可以反应得到一个六元环的分子,则A的结构简式是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酸是非常重要的工业原料,其氯代物可由乙酸和氯气在催化剂的作用下制备。实验室模拟工业生产食品香精菠萝酯(![]() ) 的简易流程如下。
) 的简易流程如下。

(1)菠萝酯的核磁共振氢谱中有__________个吸收峰。
(2)A中官能团的名称是__________。
(3)根据流程写出下列反应的化学方程式:
i.制备A: __________;该反应属于__________反应。
ii.反应室I中的反应: __________。
(4)分离室II的操作是用饱和Na2CO3溶液洗涤,而不用NaOH洗涤的原因是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚(CH3OCH3)是一种清洁能源。工业上,常利用CO2和H2合成二甲醚。有关反应如下(z、y、z均大于0):
①2CH3OH(g)CH3OCH3(g)+H2O(g) △H1= -xkJ·mol-1
②CO(g)+H2O(g)CO2(g)+H2(g) △H2= -ykJ·mol-1
③CO2(g)+3H2(g)CH3OH(g)+H2O(g) △H3= -zkJ·mol-1
(1)2CO2(g)+6H2(g)CH3OCH3(g)+3H2O(g) △H= ___________kJ·mol-1
(2)下列有关合成二甲醚的说法正确的是 ___(填字母)。
a.增大压强能提高反应速率和CO2的平衡转化率
b.体系中减小![]() ,平衡一定向正方向移动
,平衡一定向正方向移动
c.容器体积一定,混合气体密度不变时一定达到平衡状态
d.充入适量CO,可能提高CH3OCH3的产率
(3)在一定温度下,在恒容密闭容器中发生反应:CO(g)+H2O(g)CO2(g)+H2(g),速率表达式为v=v正-v逆=k正c(CO)·c(H2O)-k逆c(CO2)·c(H2O)(其中,k正、k逆为正、逆速率常数,与浓度无关)。达到平衡时,升高温度,![]() 将_____选填“增大”“减小”或“不变”)。
将_____选填“增大”“减小”或“不变”)。
(4)在恒容密闭容器中用CO2和H2合成二甲醚时CO2的平衡转化率与温度、投料比 的关系如图所示。
的关系如图所示。
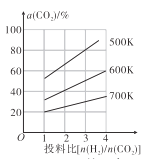
①500K时,将9mol H2和3mol CO2充入2L恒容密闭容器中,5min时反应达到平衡状态,则0~5min内的平均反应速率v(H2)=____________ molL-1min-l,该温度下,反应的平衡常数K=____(列出计算式即可,无需化简)。
②由图像可以得出的结论是_________(答两条)。
(5)工业上也可用CO和H2合成二甲醚,而且二者还能作燃料电池的燃料。以CO、H2体积比为1:2的混合气体与空气在KOH溶液中构成燃料电池(以石墨为电极),开始时,负极的电极反应式为____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.NH3 是极性分子,分子中 N 原子处在 3 个 H 原子所组成的三角形的中心
B.氨气易溶于水的原因之一是氨气分子与水分子之间能形成氢键
C.乙醇分子与水分子之间只存在范德华力
D.氯的各种含氧酸的酸性由强到弱的排列顺序为HClO>HClO2>HClO3>HClO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A.12g石墨中含有σ键的物质的量为1.5mol
B.硫离子电子共有18种运动状态,且其2p与3p轨道形状和能量相等
C.电负性:C<N<O
D.I3+离子的几何构型是V型
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】到目前为止,由化学能转变的热能或电能仍然是人类使用的最主要的能源。
(1)在25℃、101kPa下,16g的甲醇(CH3OH)完全燃烧生成CO2和液态水时放出352kJ的热量,则表示甲醇燃烧热的热化学方程式为______。
(2)化学反应中放出的热能(焓变,△H)与反应物和生成物的键能(E)有关。已知:H2(g)+Cl2(g)=2HCl(g) △H=﹣185kJ/mol,E(H﹣Cl)=432kJ/mol,E(Cl﹣Cl)=243kJ/mol则E(H﹣H)=_____。
(3)纳米级Cu2O由于具有优良的催化性能而受到关注.已知:2Cu(s)+ ![]() O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+
O2(g)═Cu2O(s)△H=﹣169kJmol﹣1,C(s)+ ![]() O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____。
O2(g)═CO(g)△H=﹣110.5kJmol﹣1,2Cu(s)+O2(g)═2CuO(s)△H=﹣314kJmol﹣1,则工业上用炭粉在高温条件下还原CuO制取Cu2O和CO的热化学方程式_____。
(4)如图是N2(g)和H2(g)反应生成2molNH3(g)过程中能量变化示意图:
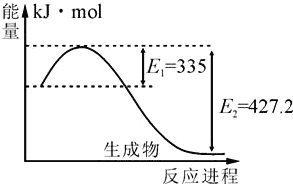
①请计算每生成1molNH3放出热量为:______。
②若起始时向容器内充入1molN2和3molH2达平衡后N2的转化率为20%,则反应放出的热量为Q1kJ,则Q1的数值为_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com