
ijͬѧ��Ҫ�õ�120 mL 1 mol/L��������Һ�������ܶ�Ϊ1��18 g/mL����������Ϊ36��5%Ũ�������ƣ���ղ���ش��������⣺
��1������1 mol/L��������Һ
��Ͳ��ȡŨ�������/mL | Ӧѡ����Ͳ�Ĺ�ɹ�ѡ��Ĺ��10 mL��25 mL��50 mL�� | Ӧѡ������ƿ�Ĺ�ɹ�ѡ��Ĺ��100 mL��250 mL��500 mL�� | ������ƿ���Ҫ���������� |
�� | �� | �� | �� |
��2������ʱ������ȷ�IJ���˳���ǣ���ĸ��ʾ��ÿ����ĸֻ����һ�Σ� __ _____��
A����30 mLˮϴ���ձ��ڱںͲ�����2��3�Σ�ϴ��Һ��ע������ƿ����
B������Ͳȷ��ȡ�����Ũ���������������õ�Ũ���ᵹ���ձ��У��ټ�������ˮ��Լ30 mL�����ò���������������ʹ���Ͼ���
C��������ȴ�������ز�����ע������ƿ��
D��������ƿ�ǽ�����ҡ��
E������������ƿ��С�ļ�ˮ��ֱ����Һ����ǡ����̶�����
��3��ָ����ʵ��IJ�������ĵط��������и��� ��
��4�������������������������ҺŨ�Ƚ��к�Ӱ�죨�ƫ�ߡ�����ƫ�͡�����Ӱ�족����
�����õ�Ũ���᳤ʱ��������ܷⲻ�õ������� ��
����������ˮʱ���������˿̶� ��
��������ʱ���ӿ̶���___________________��
������Ͳ��ȡŨ����ʱ���� ��
 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д� Ӧ����㲦ϵ�д�
Ӧ����㲦ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�������Ĵδ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��30g�ܶ�Ϊd g/mL��AlCl3����Һ�к���0.9g Al3+��������Al3+��ˮ��Ӧ������Cl-Ũ��Ϊ
A��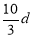 mol/L B��
mol/L B�� mol/L C��
mol/L C��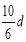 mol/L D��
mol/L D��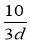 mol/L
mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����������ˮ�ķ�Ӧ�����ڹ���������ˮ�ķ�Ӧ���仯ѧ����ʽΪ��2K2O2ʮ2H2O=4KOHʮO2������0��5 mol K18O2������H2O��ȫ��Ӧ���±���������O2�������д������
K218O2������ | O2������ | |
A | 57g | O2��������9g |
B | 57g | ���ɱ�״����O2�����Ϊ5��6L |
C | 57g | O2��Ħ��������32g•mol-1 |
D | 57g | ����0��25mol O2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��㶫ʡ��������У��������ѧ�ڵ�һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
ͭпԭ��أ���ͼ������ʱ������������ȷ����

A��һ��ʱ���ͭ�����к�ɫ��������
B��������ӦΪ��Zn��2e����Zn2+
C�������·�У������Ӹ�����������
D�������е�K+����ZnSO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�찲��ʡ�쳤�и�����һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������ҩƷ��ǩ���йط�������ȷ����
ѡ�� | A | B | C | D |
��Ʒ ��ǩ | ������ˮ 1��01��105 Pa 20 �� | ҩƷ��������
| ̼������ NaHCO3 ���� С�մ� ��84 g/mol�� | Ũ���� H2SO4 �ܶ� 1��84 g/mL Ũ��98��0% |
���� | ���Լ�Ӧװ�ڲ���������ɫϸ��ƿ�� | ��ҩƷ������Ƥ��ֱ�ӽӴ� | �����������ֽ� | ������Ũ��Ϊ9��6 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
�ƿ鳤ʱ�䱩¶�ڿ����е����ղ���Ϊ
A��Na2O B��NaOH C��Na2CO3 D��Na2O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꼪��ʡ�����и�һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������100ml 1��0 mol/L Na2SO4��Һ����ȷ�ķ�����
�ٽ�32��2g Na2SO4��10H2O��������ˮ�У�����ˮϡ����100 ml
�ڽ�14��2 g Na2SO4 ����100mlˮ���Ƴ���Һ
�۽�20 ml 5��0 mol/L Na2SO4��Һ��ˮϡ����100 ml
A���٢� B���٢ڢ�
C���٢� D���ڢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016���Ĵ�ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ������
��10�֣��������⣨H2O2����ˮ��Һ�׳�˫��ˮ���������������ǵ�����������Ϊ����ɫ����������
��1��д��H2O2�ĵ���ʽ ��
��2������ΪH2O2����Ϊ����ɫ������������Ҫԭ���� ��
��3����˫��ˮ�����������ữ��FeCl2��Һ�У���Һ��dz��ɫ��Ϊ�ػ�ɫ��д���÷�Ӧ�����ӷ���ʽΪ ����Ӧ��H2O2�� ����
��4��˫��ˮ��ʹ���Ը��������Һ��ɫ���䷴Ӧ�����ӷ���ʽ���£��뽫������ʵĻ�ѧ����������ѧʽ��д�ڷ���� MnO4��+ H2O2+ H+�T Mn2++ H2O+ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ����9���¿��Ի�ѧ�Ծ��������棩 ���ͣ�ʵ����
��14�֣�ij�о���ʵ��С������֤Ũ��������Cu��Ag�Ͻ�ķ�Ӧ�����г�����NO2�����⣬����������NO���ɡ����ⶨCu��Ag�Ͻ���Cu����������������������ϱ������������£�NO2��N2O4��ϴ��ڣ��ڵ���0��ʱ����ֻ����ɫ��N2O4Һ�������ڣ���Ϊ�ˣ������������ͼ��ʾ��װ�ã�

��ش���������
��1��д��A��Cu��HNO3��Ӧ���ܵĻ�ѧ��ʽ ��
��2��ʵ�鿪ʼǰ�ȴ�A���ֵĻ���K1������ͨ��һ��ʱ��ĵ����ٹر�K1����Ŀ���� ��װ����Bƿ�������� ��
��3��ֹͣ��Ӧ��D�еĻ���K2��ͨ��O2������NO���ɣ���D�г��ֵ������� ��ʵ�鷢�֣�ͨ���O2�¶ȸߵͶ�ʵ�������нϴ�Ӱ�죬Ϊ���ڹ۲�Ӧͨ�루��ȡ����䡱�� ��O2��
��4��Ϊ��Сʵ������A�з�Ӧ��ɺ�D�г��������Ӧ�������еIJ����� ��
��5��ʵ�����������ݣ�ʵ��ǰ��Cu��Ag�Ͻ��������15.0g��ŨHNO3��40mL 13.5mol•L��1��ʵ���A��Һ��V=40mL c(H+)=1.0mol•L��1�����跴Ӧ��HNO3���ӷ�Ҳ�ֽ⣬��
�ٲμӷ�Ӧ��HNO3�����ʵ���Ϊ mol��
�����Ѳ����Ӧ��Eװ�õ��������к���Ԫ�ص���������Ϊȷ���Ͻ���Cu��������������ⶨ�������� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com