
| A. | $\frac{(a+c)}{(a+b)}$ | B. | $\frac{(a+2c)}{(a+b+c)}$ | C. | $\frac{2(a+c)}{(a+2b+c)}$ | D. | $\frac{(a+2c)}{(a+2b)}$ |
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23gNO2和N2O4的混合气体中含原子总数为1.5NA | |
| B. | 31g白磷P4(如图)中所含的P-P键的个数为0.25NA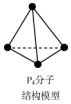 | |
| C. | 足量的Cu与100mL18.4mol/L的浓硫酸反应,失去3.68NA个电子 | |
| D. | 浓度均为2.0mol/L的盐酸和醋酸溶液各100mL,其含氢离子均为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 析出BaSO3沉淀并逸出SO3气体 | |
| B. | 析出BaSO4沉淀并逸出SO2气体 | |
| C. | 析出BaSO4和BaSO3沉淀,无气体逸出 | |
| D. | 无沉淀生成,逸出SO3和SO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 如图装置实验,一段时间后某同学记录如下:
如图装置实验,一段时间后某同学记录如下:| A. | ③④⑤ | B. | ③④ | C. | ①②③ | D. | ②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 气体NH3液体H2O | B. | 气体HCl液体H2O | ||
| C. | 气体CO2液体NaOH(aq) | D. | 气体NO液体H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com