

分析 在阿斯匹林合成中,对实验进行考查的同时,注意有机物的性质,便可解答.
(1)控制温度在85℃~90℃,小于100℃,属于水浴加热,所用玻璃仪器有:酒精灯、烧杯、温度计;
(2)晶体表面附着杂质,应洗涤除去,用冷水洗涤减少阿斯匹林因溶解而引起的损耗;
(3)加入饱和碳酸氢钠溶液使阿斯匹林转化为可溶性盐,而与不溶性的物质相互分离;
将阿斯匹林的可溶性盐重新转化为阿斯匹林,从而达到提纯的目的;
(4)水杨酸含有酚羟基,遇氯化铁溶液呈紫色,据此设计检验检验产品中是否混有水杨酸
解答 解:(1)控制温度在85℃~90℃,小于100℃,属于水浴加热,所用玻璃仪器有:酒精灯、烧杯、温度计,故答案为:水浴;酒精灯、烧杯、温度计;
(2)用冷水洗涤晶体表面附着的杂质,并且可以减少阿斯匹林因溶解而引起的损耗,故答案为:除去晶体表面附着的可溶性杂质、减少阿斯匹林的溶解;
(3)加入饱和碳酸氢钠溶液使阿斯匹林转化为可溶性盐,而与不溶性的物质相互分离;将阿斯匹林的可溶性盐重新转化为阿斯匹林,从而达到提纯的目的,故答案为:使阿斯匹林转化为可溶性盐;将阿斯匹林的可溶性盐重新转化为阿斯匹林;
(4)水杨酸含有酚羟基,遇氯化铁溶液呈紫色,具体方案为:向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸;若无紫色出现,说明产品中不含水杨酸,故答案为:向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,说明产品中有水杨酸,若无紫色出现,说明产品中不含水杨酸.
点评 本题考查有机物的合成、实验基本操作、物质的分离提纯、实验方案设计等,题目中等难度,注意掌握基本操作与有机物的性质.


科目:高中化学 来源: 题型:解答题

| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ | 5.2 | 6.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | KAl(SO4)2═K++Al3++SO42- | B. | NaH2PO4═Na++H2PO4- | ||
| C. | H2S?2H++S2- | D. | NaClO═Na++Cl-+O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 等于3:8 | B. | 大于3:8 | C. | 小于或等于3:8 | D. | 大于3:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
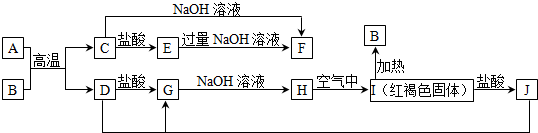
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝片与盐酸反应生成氢气 | B. | 氢氧化铝溶于强碱溶液 | ||
| C. | 氢氧化铝溶于强酸溶液 | D. | 铝热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.15NA | B. | 0.6NA | C. | 1.2NA | D. | 2.4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com