
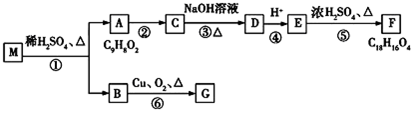
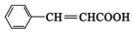 £¬EÖŠŗ¬ÓŠ¹ŁÄÜĶŵÄĆū³ĘŹĒōĒ»ł”¢ōČ»ł£®
£¬EÖŠŗ¬ÓŠ¹ŁÄÜĶŵÄĆū³ĘŹĒōĒ»ł”¢ōČ»ł£® »ņ
»ņ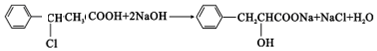 ”¢2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£®
”¢2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£®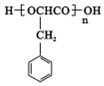 »ņ
»ņ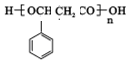 £¬ÓÉEµ¼HµÄ·“Ó¦ĄąŠĶĪŖĖõ¾Ū·“Ó¦£®
£¬ÓÉEµ¼HµÄ·“Ó¦ĄąŠĶĪŖĖõ¾Ū·“Ó¦£®·ÖĪö øł¾ŻĢāÖŠø÷ĪļÖŹ×Ŗ»Æ¹ŲĻµ£¬Čā¹šĖįŅŅõ„ŌŚĻ”ĮņĖį¼ÓČȵÄĢõ¼žĻĀ·¢ÉśĖ®½ā£ØČ”“ś£©·“Ó¦£¬øł¾ŻAµÄ·Ö×ÓŹ½æÉÖŖ£¬Bŗ¬ÓŠĮ½øöĢ¼µÄ“¼£¬BĪŖCH3CH2OH£¬B·¢ÉśŃõ»Æ·“Ӧɜ³ÉGĪŖCH3CHO£¬AĪŖōČĖį£¬±Č½ĻAŗĶFµÄ·Ö×ÓŹ½æÉÖŖ£¬·“Ó¦¢ŚĪŖ¼Ó³É·“Ó¦£¬·“Ó¦¢ŪCŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ·¢ÉśĖ®½ā£ØČ”“ś£©·“Ӧɜ³ÉD£¬·“Ó¦¢ÜDŌŁĖį»Æ£Øø“·Ö½ā·“Ó¦£©Éś³ÉE£¬·“Ó¦¢ŽEŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éś·Ö×Ó¼äõ„»Æ£ØČ”“ś£©·“Ó¦µĆF£¬F·Ö×ÓŹ½ĪŖ£ŗC18H16O4£¬ŌņEĪŖC9H10O3£¬EÖŠ²»±„ŗĶ¶Č=$\frac{9”Į2+2-10}{2}$=5£¬±½»·µÄ²»±„ŗĶ¶ČŹĒ4£¬ŌņEµÄ½į¹¹¼ņŹ½ĪŖ »ņ
»ņ £¬·“Ó¦¢ŽEŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éś·Ö×Ó¼äõ„»Æ£ØČ”“ś£©·“Ó¦µĆF£¬FĪŖ
£¬·“Ó¦¢ŽEŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éś·Ö×Ó¼äõ„»Æ£ØČ”“ś£©·“Ó¦µĆF£¬FĪŖ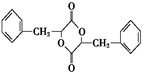 £¬
£¬
£¬DĪŖ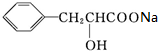 »ņ
»ņ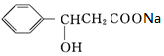 £¬CĪŖ
£¬CĪŖ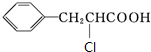 »ņ
»ņ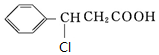 £¬AĪŖ
£¬AĪŖ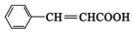 £¬½įŗĻAŗĶBµÄ½į¹¹æÉČ·¶ØMĪŖ
£¬½įŗĻAŗĶBµÄ½į¹¹æÉČ·¶ØMĪŖ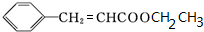 £¬¾Ż“Ė“šĢā£®
£¬¾Ż“Ė“šĢā£®
½ā“š ½ā£ŗ£Ø1£©Čā¹šĖįŅŅõ„ŌŚĻ”ĮņĖį¼ÓČȵÄĢõ¼žĻĀ·¢ÉśĖ®½ā£ØČ”“ś£©·“Ó¦£¬øł¾ŻAµÄ·Ö×ÓŹ½æÉÖŖ£¬Bŗ¬ÓŠĮ½øöĢ¼µÄ“¼£¬BĪŖCH3CH2OH£¬B·¢ÉśŃõ»Æ·“Ӧɜ³ÉGĪŖCH3CHO£¬AĪŖōČĖį£¬±Č½ĻAŗĶFµÄ·Ö×ÓŹ½æÉÖŖ£¬·“Ó¦¢ŚĪŖ¼Ó³É·“Ó¦£¬·“Ó¦¢ŪCŌŚĒāŃõ»ÆÄĘČÜŅŗÖŠ·¢ÉśĖ®½ā£ØČ”“ś£©·“Ӧɜ³ÉD£¬·“Ó¦¢ÜDŌŁĖį»Æ£Øø“·Ö½ā·“Ó¦£©Éś³ÉE£¬·“Ó¦¢ŽEŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éś·Ö×Ó¼äõ„»Æ£ØČ”“ś£©·“Ó¦µĆF£¬F·Ö×ÓŹ½ĪŖ£ŗC18H16O4£¬ŌņEĪŖC9H10O3£¬EÖŠ²»±„ŗĶ¶Č=$\frac{9”Į2+2-10}{2}$=5£¬±½»·µÄ²»±„ŗĶ¶ČŹĒ4£¬ŌņEµÄ½į¹¹¼ņŹ½ĪŖ »ņ
»ņ £¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖ£ŗōĒ»ł”¢ōČ»ł£¬·“Ó¦¢ŽEŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éś·Ö×Ó¼äõ„»Æ£ØČ”“ś£©·“Ó¦µĆF£¬FĪŖ
£¬ŗ¬ÓŠµÄ¹ŁÄÜĶÅĪŖ£ŗōĒ»ł”¢ōČ»ł£¬·“Ó¦¢ŽEŌŚÅØĮņĖį×÷ÓĆĻĀ¼ÓČČ·¢Éś·Ö×Ó¼äõ„»Æ£ØČ”“ś£©·“Ó¦µĆF£¬FĪŖ £¬
£¬
£¬DĪŖ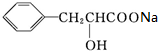 »ņ
»ņ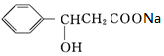 £¬CĪŖ
£¬CĪŖ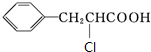 »ņ
»ņ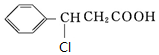 £¬AĪŖ
£¬AĪŖ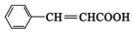 £¬
£¬
¹Ź“š°øĪŖ£ŗōĒ»ł”¢ōČ»ł£»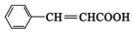 £»
£»
£Ø2£©CĪŖ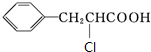 »ņ
»ņ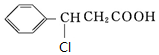 £¬·“Ó¦¢ŪĪŖĻūČ„·“Ó¦£ŗ
£¬·“Ó¦¢ŪĪŖĻūČ„·“Ó¦£ŗ »ņ
»ņ £¬BĪŖCH3CH2OH£¬B·¢ÉśŃõ»Æ·“Ӧɜ³ÉGĪŖCH3CHO£¬·“Ó¦¢ŽĪŖ£ŗ2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£¬
£¬BĪŖCH3CH2OH£¬B·¢ÉśŃõ»Æ·“Ӧɜ³ÉGĪŖCH3CHO£¬·“Ó¦¢ŽĪŖ£ŗ2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£¬
¹Ź“š°øĪŖ£ŗ »ņ
»ņ £¬
£¬
£»2CH3CH2OH+O2$”ś_{”÷}^{“߻ƼĮ}$2CH3CHO+2H2O£»
£Ø3£©EµÄ½į¹¹¼ņŹ½ĪŖ »ņ
»ņ £¬ÓÉEæÉŅŌÖʱøøß·Ö×Ó»ÆŗĻĪļH£¬ĪŖĖõ¾Ū·“Ó¦£¬HĪŖ£ŗ
£¬ÓÉEæÉŅŌÖʱøøß·Ö×Ó»ÆŗĻĪļH£¬ĪŖĖõ¾Ū·“Ó¦£¬HĪŖ£ŗ »ņ
»ņ £¬
£¬
¹Ź“š°øĪŖ£ŗ »ņ
»ņ £»Ėõ¾Ū·“Ó¦£»
£»Ėõ¾Ū·“Ó¦£»
£Ø4£©øł¾ŻÉĻĆęµÄ·ÖĪöæÉÖŖ£¬·“Ó¦¢Ł”«¢ŽÖŠ£¬ŹōÓŚČ”“ś·“Ó¦µÄŹĒ¢Ł¢Ū¢Ü¢Ż£¬¢ŚĪŖ¼Ó³É·“Ó¦£¬¢ŽĪŖŃõ»Æ·“Ó¦£¬
¹Ź“š°øĪŖ£ŗ¢Ł¢Ū¢Ü¢Ż£»
£Ø5£©BĪŖCH3CH2OH£¬IŹĒBµÄĶ¬·ÖŅģ¹¹Ģ壬ĒŅŗĖ“Ź²ÕńĒāĘ×ÖŠÖ»ÓŠŅ»øöĪüŹÕ·å£¬IĪŖ¶ž¼×ĆŃ£¬½į¹¹¼ņŹ½ĪŖCH3OCH3£¬
¹Ź“š°øĪŖ£ŗCH3OCH3£»
£Ø6£©AĪŖ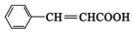 £¬1molAÓėĒāĘųĶźČ«·“Ó¦£¬ŠčŅŖĒāĘų4mol£¬±ź×¼×“æöĻĀĢå»żĪŖ89.6L£¬
£¬1molAÓėĒāĘųĶźČ«·“Ó¦£¬ŠčŅŖĒāĘų4mol£¬±ź×¼×“æöĻĀĢå»żĪŖ89.6L£¬
¹Ź“š°øĪŖ£ŗ89.6£»
£Ø7£©AĪŖ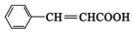 £¬ŹōÓŚ·¼Ļć×å»ÆŗĻĪļ£¬¼ČÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«£¬ĖµĆ÷ÓŠĢ¼Ģ¼Ė«¼ü£¬ÓÖÄÜÓėĢ¼ĖįĒāÄĘČÜŅŗ·“Ó¦ĖµĆ÷ÓŠōČ»ł£¬øł¾Ż·Ö×ÓŹ½æÉÖŖĪŖ-COOHÓėĢ¼Ģ¼Ė«¼ü·Ö±šĪ»ÓŚøĆČ”“ś»łµÄĮŚĪ»”¢¼äĪ»”¢¶ŌĪ»£¬ĮķŅ»ÖÖĪŖ
£¬ŹōÓŚ·¼Ļć×å»ÆŗĻĪļ£¬¼ČÄÜŹ¹äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«£¬ĖµĆ÷ÓŠĢ¼Ģ¼Ė«¼ü£¬ÓÖÄÜÓėĢ¼ĖįĒāÄĘČÜŅŗ·“Ó¦ĖµĆ÷ÓŠōČ»ł£¬øł¾Ż·Ö×ÓŹ½æÉÖŖĪŖ-COOHÓėĢ¼Ģ¼Ė«¼ü·Ö±šĪ»ÓŚøĆČ”“ś»łµÄĮŚĪ»”¢¼äĪ»”¢¶ŌĪ»£¬ĮķŅ»ÖÖĪŖ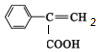 £¬ĖłŅŌĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ4ÖÖ£¬
£¬ĖłŅŌĶ¬·ÖŅģ¹¹Ģå¹²ÓŠ4ÖÖ£¬
¹Ź“š°øĪŖ£ŗ4£®
µćĘĄ ±¾ĢāŅŌČā¹šĖįŅŅõ„ĪŖŌŲĢåæ¼²é¹ŁÄÜĶÅŠŌÖŹ”¢Ķ¬·ÖŅģ¹¹Ģ唢ӊ»śŗĻ³É”¢ÓŠ»śĪļĶʶĻµČ£¬ĢāÄæÄѶČÖŠµČ£¬Ö¼ŌŚæ¼²éѧɜ¶ŌÖŖŹ¶µÄÕĘĪÕÓėĒØŅĘŌĖÓĆ”¢Ė¼Ī¬·ÖĪöµČÄÜĮ¦£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ōµē³ŲµÄøŗ¼«·¢Éś»¹Ō·“Ó¦ | |
| B£® | µē»Æѧ·“Ó¦µÄŹµÖŹŹĒ½šŹōµ„ÖŹŹ§Č„µē×ÓŠĪ³ÉŃōĄė×Ó£¬¶ųµē×ÓÖ±½ÓøųŃõ»Æ¼Į | |
| C£® | ½šŹōŌŚ³±ŹŖ»·¾³ÖŠÖ÷ŅŖ·¢ÉśĪöĒāøÆŹ“ | |
| D£® | ĶĢśŌŚ³±ŹŖµÄÖŠŠŌ»·¾³ÖŠŠāŹ“Ź±£¬æŖŹ¼ÓŠFe£ØOH£©2£¬¶ųŗóÖš½„±ä³ÉFe£ØOH£©3ŗĶFe2O3 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1 mol•L-1NaOHČÜŅŗ£ŗK+”¢Na+”¢SO42-”¢CO32- | |
| B£® | ÄÜÓėĀĮ·“Ó¦·Å³öĒāĘųµÄČÜŅŗÖŠ£ŗK+”¢SO42-”¢NO3-”¢NH4+ | |
| C£® | 0.1 mol•L-1FeCl3ČÜŅŗ£ŗK+”¢NH4+”¢I-”¢SCN- | |
| D£® | c£ØH+£©/c£ØOH-£©=1”Į1014µÄČÜŅŗ£ŗCa2+”¢Na+”¢ClO-”¢NO3- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | pHÖµ¶¼ĪŖ4µÄĻ”ŃĪĖįŗĶNH4ClČÜŅŗÖŠ£¬Ė®µÄµēĄė³Ģ¶ČĻąĶ¬ | |
| B£® | ÅØ¶Č¾łĪŖ0.1mol/LµÄ“×ĖįŗĶNaOHČÜŅŗµČĢå»ż»ģŗĻŗó£ŗlg[$\frac{c£Ø{H}^{+}£©}{c£ØO{H}^{-}£©}$]=0 | |
| C£® | ŌŚŗ¬ÅØ¶Č¶¼ĪŖ0.01mol/LµÄCl-”¢CrO42-µÄ»ģŗĻČÜŅŗÖŠµĪ¼ÓAgNO3ČÜŅŗ£¬ĻČ³öĻÖ³ĮµķµÄŹĒAgCl£®[ŅŃÖŖ£ŗKsp£ØAgCl£©=1.8”Į10-10£¬Ksp£ØAg2CrO4£©=1.9”Į10-12] | |
| D£® | ÅØ¶Č¾łĪŖ0.1mol/LµÄNH4ClŗĶCH3COONH4ČÜŅŗÖŠ£¬c£ØNH4+£©ĻąĶ¬ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
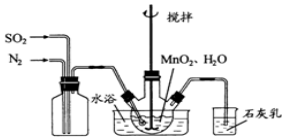
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CuSO4 | B£® | BaCl2 | C£® | NaNO3 | D£® | H2SO4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
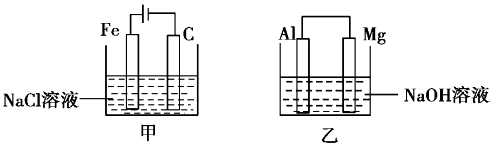
| A£® | ¼××°ÖĆÖŠÓŠ³ĮµķÉś³É£¬ŅŅ×°ÖĆÖŠMgµē¼«ÉĻÓŠĘųÅŻÉś³É | |
| B£® | ·“Ó¦ŗ󣬼××°ÖĆÖŠČÜŅŗµÄÖŹĮæŌö“ó£¬ŅŅ×°ÖĆÖŠČÜŅŗµÄÖŹĮæ¼õŠ” | |
| C£® | µē¼«·“Ó¦Ź½£ŗ¼×ÖŠŃō¼«Fe-2e-=Fe2+£¬ŅŅÖŠøŗ¼«Mg-2e-=Mg2+ | |
| D£® | ·“Ó¦ŗó¼×ÖŠČÜŅŗµÄpH¼õŠ”£¬ŅŅÖŠČÜŅŗµÄpHŌö“ó |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com