
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
A£®ĢśŹĒĪ»ÓŚµŚĖÄÖÜĘŚµŚ¢ųB×åŌŖĖŲ, ŹĒŅ»ÖÖÖŲŅŖµÄ¹ż¶ÉŌŖĖŲ
B£®ĖÄŃõ»ÆČżĢśŹĒŃõ»ÆĢśŗĶŃõ»ÆŃĒĢś×é³ÉµÄ»ģŗĻĪļ
C£®14æĖĢś·ŪŗĶ7æĖĮņ·Ū»ģŗĻŗóøßĪĀĻĀ³ä·Ö·“Ó¦ÄÜÉś³É21æĖĮņ»ÆŃĒĢś
D£®ĢśŌŚäåÕōĘųÖŠµćČ¼æÉÉś³ÉFeBr3

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
X”¢Y”¢Z”¢Q”¢MĪŖ³£¼ūµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĘäŌ×ÓŠņŹżŅĄ“ĪŌö“ó”£ÓŠ¹ŲŠÅĻ¢ČēĻĀ±ķ:
| X | ¶ÆÖ²ĪļÉś³¤²»æÉȱɣµÄŌŖĖŲ£¬ŹĒµ°°×ÖŹµÄÖŲŅŖ³É·Ö |
| Y | µŲæĒÖŠŗ¬Įæ¾ÓµŚŅ»Ī» |
| Z | ¶ĢÖÜĘŚÖŠĘäŌ×Ó°ė¾¶×ī“ó |
| Q | Éś»īÖŠ“óĮæŹ¹ÓĆĘäŗĻ½šÖĘĘ·£¬¹¤ŅµÉĻæÉÓƵē½āĘäŃõ»ÆĪļµÄ·½·ØÖʱø |
| M | ŗ£Ė®ÖŠ“óĮæø»¼ÆµÄŌŖĖŲÖ®Ņ»£¬Ęä×īøßÕż»ÆŗĻ¼ŪÓėøŗ¼ŪµÄ“śŹżŗĶĪŖ6 |
£Ø1£©XµÄĘųĢ¬Ēā»ÆĪļµÄ“óĮæÉś²śŌų¾½ā¾öĮĖµŲĒņÉĻŅņĮøŹ³²»×ć¶ųµ¼ÖĀµÄ¼¢¶öŗĶĖĄĶöĪŹĢā£¬ĒėŠ“³öøĆĘųĢ¬Ēā»ÆĪļµÄµē×ÓŹ½____________”£
£Ø2£©ŅŃÖŖ37RbŗĶ53I¶¼Ī»ÓŚµŚĪåÖÜĘŚ£¬·Ö±šÓėZŗĶMĶ¬Ņ»Ö÷×唣ĻĀĮŠÓŠ¹ŲĖµ·ØÕżČ·µÄŹĒ____________£ØĢīŠņŗÅ£©”£
A£®Ō×Ó°ė¾¶£ŗ Rb>I B£®RbMÖŠŗ¬ÓŠ¹²¼Ū¼ü
C£®ĘųĢ¬Ēā»ÆĪļČČĪČ¶ØŠŌ£ŗM>I
D£®Rb”¢Q”¢MµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļæÉŅŌĮ½Į½·¢Éś·“Ó¦
¢ĒČōXM3×ī³õĖ®½ā²śĪļŹĒXH3ŗĶHMO£¬ŌņX”¢MŌŖĖŲµÄµēøŗŠŌ“óŠ”Ė³ŠņŹĒ:X_____M(£ØĢī£¾”¢£¼”¢»ņ=)£»ČōŅŃÖŖĮ×ÓėMŌŖĖŲµēøŗŠŌ¹ŲĻµŹĒ£ŗP£¼M£¬ŌņPM3Ė®½āµÄ»Æѧ·“Ó¦·½³ĢŹ½ŹĒ ”£
£Ø4£©ŅŃÖŖQM3µÄČŪµćĪŖ190”ę(2.02”Į105Pa)£¬µ«ĖüŌŚ180”ę¼“æŖŹ¼Éż»Ŗ£¬ŌņQM3ŹĒ_________(Ģī”°Ąė×Ó»ÆŗĻĪļ”±»ņ”°¹²¼Ū»ÆŗĻĪļ”±)£¬ČēŗĪĶعżŹµŃéÅŠ±š__________________”£ŌŚ500KŗĶ1.01”Į105PaŹ±£¬ĖüµÄÕōĘųĆܶČ(»»Ėć³É±ź×¼×“æöŹ±)ĪŖ11.92g/L£¬ŌņQM3µÄ½į¹¹Ź½ĪŖ_________”£
£Ø5£©X”¢Y×é³ÉµÄŅ»ÖÖĪŽÉ«ĘųĢåÓöæÕĘų±äĪŖŗģ×ŲÉ«”£½«±ź×¼×“æöĻĀ40 £ĢøĆĪŽÉ«ĘųĢåÓė15 £ĢŃõĘųĶØČėŅ»¶ØÅØ¶ČµÄNaOHČÜŅŗÖŠ£¬Ē”ŗƱ»ĶźČ«ĪüŹÕ£¬Ķ¬Ź±Éś³ÉĮ½ÖÖŃĪ”£ĒėŠ“³öøĆ·“Ó¦µÄĄė×Ó·½³ĢŹ½ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
Š”Ć÷Ģå¼ģµÄŃŖŅŗ»ÆŃ鵄֊£¬ĘĻĢŃĢĒĪŖ5.9”Į10-3mol/L”£±ķŹ¾øĆĢå¼ģÖø±źµÄĪļĄķĮæŹĒ
A£®Čܽā¶Č(s) B£®ĪļÖŹµÄĮæÅضČ(c) C£®ÖŹĮæ·ÖŹż(w) D£®Ä¦¶ūÖŹĮæ(M)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ

 ĻÖÓŠĻĀĮŠĪļÖŹ£ŗ¢ŁNa2CO3•10H2O¾§Ģå ¢ŚŠæ ¢ŪĀČ»ÆĒā ¢ÜCO2 ¢ŻNaHSO4¹ĢĢå ¢ŽBa(OH)2 ¹ĢĢå ¢ßŗģŗÖÉ«µÄĒāŃõ»ÆĢśŅŗĢå ¢ą°±Ė® ¢įĻ”ĮņĖį ¢āČŪČŚNaCl ¢Ļ ÕįĢĒ £Ø1£©°“ĪļÖŹµÄ·ÖĄą·½·ØĢīŠ“±ķøńµÄæհד¦ (Ģī±ąŗÅ) £ŗ
ĻÖÓŠĻĀĮŠĪļÖŹ£ŗ¢ŁNa2CO3•10H2O¾§Ģå ¢ŚŠæ ¢ŪĀČ»ÆĒā ¢ÜCO2 ¢ŻNaHSO4¹ĢĢå ¢ŽBa(OH)2 ¹ĢĢå ¢ßŗģŗÖÉ«µÄĒāŃõ»ÆĢśŅŗĢå ¢ą°±Ė® ¢įĻ”ĮņĖį ¢āČŪČŚNaCl ¢Ļ ÕįĢĒ £Ø1£©°“ĪļÖŹµÄ·ÖĄą·½·ØĢīŠ“±ķøńµÄæհד¦ (Ģī±ąŗÅ) £ŗ
| ·ÖĄą±ź×¼ | Äܵ¼µēµÄĪļÖŹ | µē½āÖŹ | ·Ēµē½āÖŹ |
| ŹōÓŚøĆĄąµÄĪļÖŹ |
|
 £Ø2£©ÉĻŹöĪļÖŹÖŠÓŠĪļÖŹÖ®¼äŌŚČÜŅŗÖŠæÉ·¢ÉśĄė×Ó·“Ó¦£ŗH£«£«OH£ØTØTH2O£¬Š“³öŅ»øöøĆĄė×Ó·“Ó¦¶ŌÓ¦µÄ»Æѧ·½³ĢŹ½
£Ø2£©ÉĻŹöĪļÖŹÖŠÓŠĪļÖŹÖ®¼äŌŚČÜŅŗÖŠæÉ·¢ÉśĄė×Ó·“Ó¦£ŗH£«£«OH£ØTØTH2O£¬Š“³öŅ»øöøĆĄė×Ó·“Ó¦¶ŌÓ¦µÄ»Æѧ·½³ĢŹ½
£Ø3£©½«¢įµĪ¼Óµ½¢ßÖŠÖĮ¹żĮæµÄŹµŃéĻÖĻóŹĒ
£Ø4£©½«¢ŪĶØČė¢ąÖŠÖĮĒ”ŗĆĶźČ«·“Ó¦£¬ŌņČÜŅŗµ¼µēÄÜĮ¦µÄ±ä»ÆĪŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠø÷»Æѧ·“Ó¦µÄĄė×Ó·½³ĢŹ½ÖŠ£¬ÓŠ“ķĪóµÄŹĒ£Ø £©
A£®ĀĮÓėĒāŃõ»ÆÄĘ·“Ó¦£ŗ2Al+2OH£+2H2O=2AlO2£+3 H2”ü
B£®Ńõ»ÆĀĮČÜÓŚĒāŃõ»ÆÄĘČÜŅŗ£ŗAl2O3+2OH£=2AlO2£+H2O
C£®µā»ÆŃĒĢśČÜŅŗÖŠµĪČė×ćĮæäåĖ®£ŗ2Fe2++2I£+2Br2=I2+2Fe3++4Br£
D£®Ģ¼ĖįĒāĆ¾ČÜŅŗÖŠ¼Ó¹żĮæ³ĪĒåŹÆ»ŅĖ®
Mg2++2HCO3£+2Ca2++4OH£=2CaCO3”ż+2H2O+Mg£ØOH£©2”ż
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
ĻĀĮŠĖł×÷³öµÄ½įĀŪÖŠŅ»¶ØÕżČ·µÄŹĒ£Ø””””£©
A£®ĪŽÉ«ŹŌŅŗŹ¹ŗģÉ«ŹÆČļŹŌÖ½±äĄ¶£¬½įĀŪ£ŗøĆŹŌŅŗŅ»¶ØŹĒ¼īČÜŅŗ
B£®¼ÓČėĀČ»Æ±µČÜŅŗÓŠ°×É«³Įµķ²śÉś£¬ŌŁ¼ÓŃĪĖį£¬³Įµķ²»ĻūŹ§£¬Ņ»¶ØÓŠSO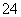
C£®ĪŽÉ«ŹŌŅŗŃęÉ«·“Ó¦³Ź»ĘÉ«£¬½įĀŪ£ŗŹŌŅŗÖŠŅ»¶Øŗ¬ÓŠNa£«
D£®ĪŽÉ«ŹŌŅŗ¼ÓČėĢ¼ĖįÄĘČÜŅŗ²śÉś°×É«³Įµķ£¬½įĀŪ£ŗŹŌŅŗÖŠŗ¬ĒāŃõ»ÆøĘ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
¢ń£®¶žŃõ»ÆĪų£ØSeO2£©ŹĒŅ»ÖÖŃõ»Æ¼Į£¬Ęä±»»¹ŌŗóµÄµ„ÖŹĪųæÉÄܳÉĪŖ»·¾³ĪŪČ¾Īļ£¬ĶعżÓėÅØHNO3»ņÅØH2SO4·“Ӧɜ³ÉSeO2ŅŌ»ŲŹÕSe”£
Ķź³ÉĻĀĮŠĢīæÕ£¬
£Ø1£©SeŗĶÅØHNO3·“Ó¦µÄ»¹Ō²śĪļĪŖNOŗĶNO2£¬ĒŅNOŗĶNO2µÄĪļÖŹµÄĮæÖ®±ČĪŖ1£ŗ1£¬Š“³öSeŗĶÅØHNO3µÄ·“Ó¦·½³ĢŹ½ ”£
Čē²»¶ŌøĆ·“Ó¦»¹Ō²śĪļµÄ±ČĄż×÷ĻŽÖĘ£¬øĆ·“Ó¦ ³öĻÖ¶ą×éÅäĘ½ĻµŹż£ØĢī”°æÉÄÜ”±»ņ”°²»æÉÄÜ”±£©²¢ĖµĆ÷ĄķÓÉ ”£
£Ø2£©»ŲŹÕµĆµ½µÄSeO2µÄŗ¬Į棬æÉŅŌĶعżĻĀĆęµÄ·½·Ø²ā¶Ø£ŗ
¢ŁSeO2+KIŹ®HNO3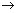 Se+I2+KNO3Ź®H2O
Se+I2+KNO3Ź®H2O
¢ŚI2+2Na2S2O3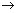 Na2S4O6+2NaI
Na2S4O6+2NaI
ŹµŃéÖŠ£¬×¼Č·³ĘĮæSeO2ѳʷ0.160 0 g£¬ĻūŗÄĮĖ0.200 0 mol L-1µÄNa2S2O3ČÜŅŗ25.00mL£¬Ėł²ā¶ØµÄѳʷ֊SeO2µÄÖŹĮæ·ÖŹżĪŖ
L-1µÄNa2S2O3ČÜŅŗ25.00mL£¬Ėł²ā¶ØµÄѳʷ֊SeO2µÄÖŹĮæ·ÖŹżĪŖ
¢ņ£®øßĢśĖį¼Ų£ØK2FeO4£©ŹĒŅ»ÖÖ¼ÆŃõ»Æ”¢Īüø½”¢ŠõÄż”¢ÖśÄż”¢É±¾ś”¢³ż³ōĪŖŅ»ĢåµÄŠĀŠĶøߊ§¶ą¹¦ÄÜĀĢÉ«Ė®“¦Ąķ¼Į£¬¾ßÓŠĮ¼ŗƵÄÓ¦ÓĆĒ°¾°”£ĘäÉś²ś¹¤ŅÕČēĻĀ£ŗ
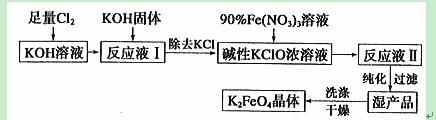
ŅŃÖŖ£ŗ¢Ł2KOH+Cl2 KCl+KClO+H2O£ØĢõ¼ž£ŗĪĀ¶Č½ĻµĶ£©
KCl+KClO+H2O£ØĢõ¼ž£ŗĪĀ¶Č½ĻµĶ£©
¢Ś6KOH+3C12 5KCl+KClO3+3H2O£ØĢõ¼ž£ŗĪĀ¶Č½Ļøߣ©
5KCl+KClO3+3H2O£ØĢõ¼ž£ŗĪĀ¶Č½Ļøߣ©
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©øĆÉś²ś¹¤ŅÕÓ¦ŌŚ £ØĢī”°ĪĀ¶Č½ĻøߔƔƻņ”°ĪĀ¶Č½ĻµĶ”±£©µÄĒéæöĻĀ½ųŠŠ”£
£Ø2£©Š“³öFe£ØNO3£©3ŌŚĒæ¼īŠŌĢõ¼žĻĀÓėKClO·“Ó¦ÖĘK2FeO4µÄĄė×Ó·½³ĢŹ½ ”£
£Ø3£©ŌŚ”°·“Ó¦Ņŗ¢ń”±ÖŠ¼ÓKOH¹ĢĢåµÄÄæµÄŹĒ £ØĢīŠņŗÅ£©”£
A£®Óė”°·“Ó¦Ņŗ¢ń”±ÖŠ¹żĮæµÄCl2¼ĢŠų·“Ó¦£¬Éś³Éøü¶ąµÄKClO
B£®KOH¹ĢĢåČܽāŹ±»į·Å³ö½Ļ¶ąµÄČČĮ棬ӊĄūÓŚĢįøß·“Ó¦ĖŁĀŹ
C£®ĪŖĻĀŅ»²½·“Ó¦Ģį¹©·“Ó¦Īļ
D£®Ź¹ø±²śĪļKClO3»ÆĪŖKClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
½«20 mL 0.3 mol/L AgNO3ČÜŅŗÓė10 mL 0.4 mol/L CaCl2ČÜŅŗ»ģŗĻ£¬ĖłµĆČÜŅŗÖŠĄė×ÓÅØ¶Č¹ŲĻµÕżČ·µÄŹĒ
A. c(NO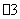 )£¾c(Ca2+)£¾c(Cl£) B. c(Ca2+)£¾c(NO
)£¾c(Ca2+)£¾c(Cl£) B. c(Ca2+)£¾c(NO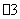 )£¾c(Cl£)
)£¾c(Cl£)
C. c(Ca2+)£¾c(Cl£)£¾c(NO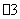 ) D. c(Cl£)£¾c(Ca2+)£¾c(NO
) D. c(Cl£)£¾c(Ca2+)£¾c(NO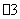 )
)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
»ÆŗĻĪļA”¢BŹĒ֊ѧ³£¼ūµÄĪļÖŹ£¬ĘäŅõ”¢ŃōĄė×ÓÖ»ÄÜ“ÓĻĀ±ķÖŠŃ”Ōń£ŗ
| ŃōĄė×Ó | K£«”¢Na£«”¢Fe2£«”¢Ba2£«”¢NH |
| ŅõĄė×Ó | OH£”¢NO |
(1)ČōA”¢BµÄĖ®ČÜ Ņŗ¾łĪŖĪŽÉ«£¬ĒŅAµÄĖ®ČÜŅŗ³ŹĒæĖįŠŌ£¬BµÄĖ®ČÜŅŗ³ŹĒæ¼īŠŌ”£»ģŗĻŗó²śÉś²»ČÜÓŚĻ”ŃĪĖįµÄ°×É«³Įµķ¼°ÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«µÄĘųĢ唣
Ņŗ¾łĪŖĪŽÉ«£¬ĒŅAµÄĖ®ČÜŅŗ³ŹĒæĖįŠŌ£¬BµÄĖ®ČÜŅŗ³ŹĒæ¼īŠŌ”£»ģŗĻŗó²śÉś²»ČÜÓŚĻ”ŃĪĖįµÄ°×É«³Įµķ¼°ÄÜŹ¹ŹŖČóµÄŗģÉ«ŹÆČļŹŌÖ½±äĄ¶É«µÄĘųĢ唣
¢ŁBµÄ»ÆѧŹ½ĪŖ__________________________________________________________”£
¢ŚA”¢BČÜŅŗ»ģŗĻ¼ÓČČ·“Ó¦µÄĄė×Ó·½³ĢŹ½_____________________________________”£
(2)ČōAµÄĖ®ČÜŅŗ³ŹĒ³ĀĢÉ«£¬BµÄĖ®ČÜŅŗĪŽÉ«ĒŅĘäŃęÉ«·“Ó¦ĪŖ»ĘÉ«”£ĻņAµÄĖ®ČÜŅŗÖŠ¼ÓČėĻ”ŃĪĖįĪŽĆ÷ĻŌĻÖĻó£¬ŌŁ¼ÓČėBŗóČÜŅŗ±ä»Ę£¬µ«A”¢BµÄĖ®ČÜŅŗ»ģŗĻŅąĪŽĆ÷ĻŌ±ä»Æ”£Ōņ
¢ŁAµÄ»ÆѧŹ½ĪŖ__________________________________________________________”£
¢Ś¾·Ö ĪöÉĻŹö¹ż³ĢÖŠČÜŅŗ±ä»ĘµÄŌŅņæÉÄÜÓŠĮ½ÖÖ(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)
ĪöÉĻŹö¹ż³ĢÖŠČÜŅŗ±ä»ĘµÄŌŅņæÉÄÜÓŠĮ½ÖÖ(ÓĆĄė×Ó·½³ĢŹ½±ķŹ¾)
¢ń________________________________________________________________________£»
¢ņ________________________________________________________________________”£
¢ŪĒėÓĆŅ»¼ņŅ×·½·ØÖ¤Ć÷ÉĻŹöČÜŅŗ±ä»ĘµÄŌŅņ___________________________________”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com