
焦炭是工业生产中的重要还原剂和燃料,活性炭用于生活和实验室中通过吸附作用除去有害气体或有毒物质。它们的化学成分都可以看成是碳单质。
(1)红热的焦炭投入浓硝酸中,写出反应的化学方程式 ;
(2)将一定条件下的高锰酸钾溶液与活性炭混合,可发生如下反应(未配平) MnO4-+ C+ H2O—— MnO2+ ① +CO32-,则 ① 处应该填入的微粒化学式为 ;
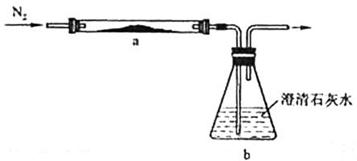 (3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
(3)PbO俗称密陀僧或铅黄,将黄色粉末状PbO和足量活性炭充分混合,平铺在反应管a中,在b瓶中盛足量澄清石灰水,按图连接仪器。实验开始时缓缓通入氮气,过一段时间后,加热反应管a,观察到管内发生剧烈反应,并有熔融物生成。同时,b瓶的溶液中出现白色浑浊。待反应完全后,停止加热,仍继续通氮气,直至反应管冷却。此时,管中的熔融物凝固成银白色金属。
写出反应管a中发生的所有反应的化学方程式
 考前必练系列答案
考前必练系列答案科目:高中化学 来源: 题型:
已知H2(g)+I2(g)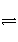
 2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
2HI(g) ΔH<0。有相同容积的定容密闭容器甲和乙,甲中加入H2和I2各0.1 mol,乙中加入HI 0.2 mol,相同温度下分别达到平衡。欲使甲中HI的平衡浓度大于乙中HI的平衡浓度,应采取的措施是( )
A.甲、乙提高相同温度
B.甲中加入0.1 mol He,乙不变
C.甲降低温度,乙不变
D.甲增加0.1 mol H2,乙增加0.1 mol I2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.1 mol H2O的质量为18 g/mol
B.CH4的摩尔质量为16 g
C.3.01×1023个SO2分子的质量为32 g
D.标准状况下,1 mol任何物质体积约为22.4 L
查看答案和解析>>
科目:高中化学 来源: 题型:
化学为人类基本的生存需要、进而追求生活乃至生命质量的提升提供了重要的保障。但某些人的贪得无厌和对化学原理的滥用败坏了化学学科声誉,我们每个人都应该避免成为这样的人。下列科学史上的重要发现与发明,从原理上看与化学学科没有直接相关性的是
A、1774年舍勒最早制得氯气,1820年前后漂白粉用于饮用水消毒
B、1869年门捷列夫发现元素周期律,使元素的性质更有规律可循
C、1902年哈伯开始对合成氨反应进行研究,工业化后提高了粮食产量
D、1942年费米进行了235U原子核裂变试验,从而开创原子能利用时代
查看答案和解析>>
科目:高中化学 来源: 题型:
海带中碘元素的检验可经过以下四个步骤完成,各步骤中选用的实验用品不能都用到的是


A.将干海带剪碎后灼烧灰化,选用①、②和⑨
B.将海带灰加入蒸馏水搅拌煮沸,选用④、⑥和⑦
C.过滤得到的滤液,选用④、⑤和⑦
D.检验滤液中的I-,选用③、⑧和⑩
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,下列叙述不是可逆反应A(g)+3B(g)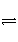
 2C(g)达到平衡状态标志的是( )
2C(g)达到平衡状态标志的是( )
①C生成的速率与C分解的速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④A、B、C的压强不再变化
⑤混合气体的总压强不再变化
⑥混合气体的物质的量不再变化
⑦单位时间内消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
A.②⑧ B.①⑥ C.②④ D.③⑧
查看答案和解析>>
科目:高中化学 来源: 题型:
2SO2(g)+O2(g) 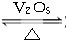 2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
2SO3(g)是制备硫酸的重要反应。下列叙述正确的是( )
A.催化剂V2O5不改变该反应的逆反应速率
B.增大反应体系的压强,反应速率一定增大
C.该反应是放热反应,降低温度将缩短反应达到平衡的时间
D.在t1、t2时刻,SO3(g)的浓度分别是c1,c2,则时间间隔t1~t2内,SO3(g)生成的平均速率为v=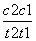
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质应用的说法正确的是( )
A.碳酸钠溶液呈碱性,可用热的纯碱溶液除去矿物油污渍
B.钠和钾的合金在常温下是液体,可用于快中子反应堆作热交换剂
C.常温下,浓硝酸不跟铁发生化学反应,可用铁制容器盛装浓硝酸
D.铝表面易形成致密的氧化膜,铝制器皿可长时间盛放咸菜等腌制食品
查看答案和解析>>
科目:高中化学 来源: 题型:
下表列出了①~⑦七种元素在周期表中的位置:
|
| ⅠA | 0 | ||||||
| 1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ |
请按要求回答下列问题。
(1)元素④在周期表中的位置是第______周期,第________族。
(2)①、⑤、⑥三种元素的最高价氧化物对应的水化物中,碱性最强的是__________(填化学式)。
(3)元素③属于___________(填金属或非金属)元素,它的最高正化合价是__________,
它的单质与H2在一定条件下反应生成化合物X,X的水溶液显__________(填酸性,碱性或中性)。
(4)元素⑤与元素⑦形成的化合物中化学键的类型是____________。
(5)画出元素⑥的原子结构示意图 ,它的单质_________(填能或不能)与氢氧化钠溶液反应。
(6)元素②形成的最简单的有机物的分子式为______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com